Energy and Enzymes
Metabolism 是指細胞中一連串的 chemical reaction,它們可以用來儲存、釋放、轉換 energy,並且可以建構和破壞複雜的 molecules,例如 sugar, proteins, DNA 等等。這些 chemical reaction 都需要一種 protein 稱作 enzyme 來 facilitate 和 catalyze,以便正確的發生這些 reaction。例如,cellular respiration 使用 enzyme 來將 glucose 分解成 ATP,而 photosynthesis 則是把太陽的能量轉換成 glucose。
Overview of metabolism
- 細胞正無時無刻的運作上千種 chemical reaction 來讓身體保持正常
- 這些一連串的 chemical reaction 又稱為 cell's metabolism
- 例如下圖是一個 eukaryotic cell 的 metabolic pathways
- 每條線是一個 reaction
- 每個點是 reactant 或 product
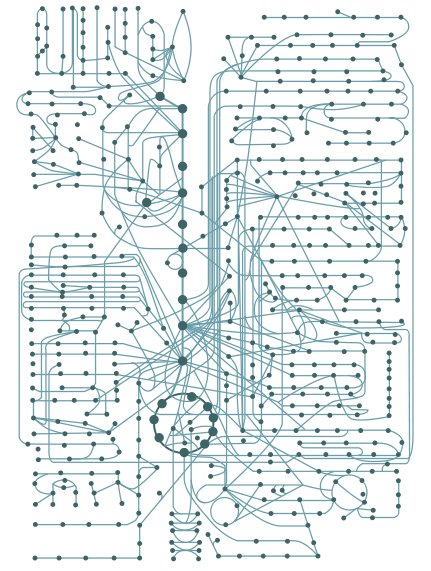
- 在 cell 中的 metabolic web 的 chemical reaction 會釋放能量而且可能會自發性的發生
- 但有的需要外部的 energy 來讓 reaction 發生
- 事實上,我們吃的食物就是用來產生 reaction 的 energy
- 在來要介紹兩個非常重要的 metabolic processes
- build & break down sugars
Breaking down glucose: Cellular respiration
- 這是一個 energy-releasing pathway 的範例
- 將吃的點心中的 sugar molecules 分解來使用
- 我們身體大多數的 cell 都是用 glucose 來獲得能量
- 這個過程稱為 cellular respiration
- 這個過程細分成非常多小步驟,但可以用底下的化學式統整
- 分解 glucose 產生的 energy,會被細胞以 ATP 的形式捕捉起來
- ATP 分子的全名為 adenosine triphosphate
- ATP 是一個小分子用來讓 cell 可以更方便儲存能量
- 可以將 ATP 想像成 cell 的 energy 貨幣 (energy currency of the cell)
- 有了 ATP,其他需要 energy 的 reaction 就可以使用他
Building up glucose: Photosynthesis
- 我們已經知道 sugar 可以分解成 ATP,那 sugar 是如何組成的呢
- sugar (e.g., glucose) 主要由植物執行 photosynthesis 來生成
- 植物使用太陽的能量,一樣一步步的將 carbon dioxide gas 轉換成 sugar molecules
- 一樣非常多步驟,但可以用一個化學式統整 (其實就是 cellular respiration 的相反)
- 植物除了本身需要 energy (sugar) 來執行自己的 cellular processes
- 但植物也提供了 food source 給動物們
- 這些食物就會透過 cellular respiration 從 glucose 分解成 ATP 供細胞運作
Anabolic and catabolic pathways
- 不管是組合或拆解 glucose 都是 metabolic pathway 的一種
- metabolic pathway 就是一連串的 chemical reaction 互相照顧彼此
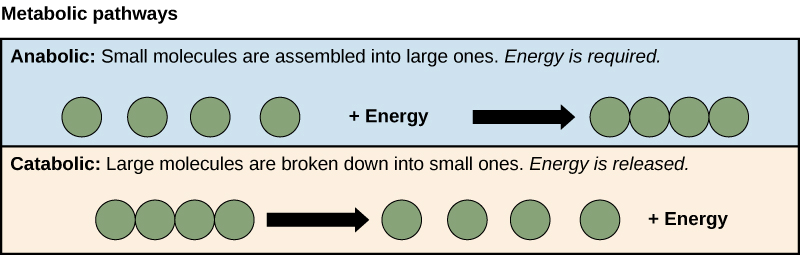
- Metabolic pathways 又可以依照 effects 被分為兩大類
- Anabolic (anabolism) 指的是 building up
- Catabolic (catabolism) 指的是 breaking down
- Metabolic pathways 中的 chemical reactions 不是自動自發、毫無頭緒的在運作
- 通常由一種 protein 稱作 enzyme 來 facilitate, catalyze 這些 reaction
Anabolic pathways
- 將簡單的 molecules 組裝成複雜的 molecules,通常需要 energy inputs
- Carbon dioxide 組裝成 glucose
- Amino acids 組裝成 proteins
- nucleotides 組裝成 DNA strands
- 這些 "biosynthetic process" 所用的 energy 通常為 ATP 或其他 short-term energy storage molecules
Catabolic pathways
- 將複雜的 molecules 分解成簡單的 molecules,通常也會釋放 energy
- 例如釋放儲存在 glucose, fats 的 energy
- 得到這些 energy 就可以轉換成適合使用的格式,例如 ATP
Types of Energy
- 這邊指的 energy 不是起床很有精神那種 energy
- 這邊指的 energy 是定義為 ability to do work
- 例如 light, heat, electrical energy
- 我們來詳細了解一下 biological system 中幾個重要的 energy
- kinetic energy (motion)
- potential energy (position, structure)
- chemical energy (chemical bonds 的 potential energy)
- 要注意的是 energy 永遠不會消失,只會從一種型態轉換成另一種
Kinetic energy
- 物體移動產生的能量就稱為 kinetic energy (動能)
- speeding bullet, walking person, electromagnetic radiation (light) 都有
- Thermal energy 也是一種 kinetic energy
- 來自 atoms 或 molecules 隨機跳動時產生
- 一群 molecules 的 average thermal energy 就是 temperature
- 而當 thermal energy 在兩個物體轉移時,就是 heat
Potential energy
- 跟物體本身的架構或位置有關的則稱為 potential energy (位能、勢能)
- 水庫的水、跳傘的人、拆房子的鐵球
- Chemical energy 也是一種 potential energy
- 指的是存在 chemical bonds 的 energy
- 位能表示了物體在特定位置上所儲存的能量,在適當情況下,位能可以轉換為動能
Energy conversions
- 當鐵球被起重機拉到高空停止時
- 這時鐵球的 kinetic energy 不存在
- 但鐵球的 potential energy 非常大
- 這時鐵球被釋放,因為重力的關係高速的向下掉
- 下降時 kinetic energy 越來越來越大
- 但 potential energy 則是減少到幾乎不存在
Energy in car
- Chemical energy (potential) 的 conversions 在日常中也可以看到
- 例如 gasoline 中的 octane (hydrocarbon) 含有 chemical energy
- 汽車引擎中的 gasoline combust 將會釋放這些 energy
- 產生的 high-temperature gases 將會推動 pistons 然後讓車前進 (kinetic energy)
- 所以一些 chemical energy 轉換成 kinetic energy
- 而一些 chemical energy 則會轉換成 thermal energy (heat emitted from engine)
Energy in life
- Energy 會儲存在 ATP 的 bonds 當中 (potential energy)
- 這些 energy 可以轉換成 kinetic energy
- 例如移動 motor protein
- 收縮 muscle cells 來移動四肢
The Laws of Thermodynamics
- 人是一個 open system (幾乎所有生物都不是 closed system)
- 意思是我們總會和周遭環境交換 matter, energy
- 例如從食物獲得 chemical energy
- 然後透過 moving, talking, walking, breathing 對周遭 do work (做功)
- 意思是我們總會和周遭環境交換 matter, energy
- 所有 energy 的交換 (體內外) 都可以被定義為 laws of physics
- 例如在 hot, cold, gas molecules 等情況下的 energy 交換
- 所以接下來先來看兩個 laws - first and second laws of thermodynamics
Systems and surroundings
- Biology 的 thermodynamics 指的是一個或一群 molecules 的 energy transfer
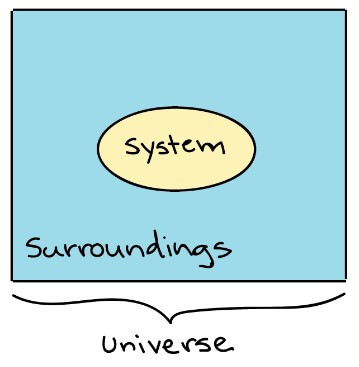
- 這時我們關心的那群東西 (小到 molecules 大到 ecosystem) 都稱為 system
- 其他不在 system 的東西就稱為 surroundings
- 兩者相加就是 universe
Thermodynamics 有三種 system
- Open system
- 可以和 surroundings 交換 energy 和 matter
- Closed system
- 只能和 surroundings 交換 energy,不能交換 matter
- Isolated system
- 什麼都不能和 surroundings 交換
- 只有和內部的 items 交換
- Open system
所以人是 open system,吃和做任何事都是在跟 surroundings 交換 energy, matter
- 這些交換都是要遵守 laws of physics 的
- 可以說人和周遭進行的 energy 交換,就跟 circuit 中電流交換一模一樣
- Laws of thermodynamics 就是 energy transfer 的 physical rules
The First Law of Thermodynamics
第一個法則的範圍超級大,探討的是整個宇宙的 energy
- 整個宇宙的 energy total amount 是不變的
- 所以 energy 不能被 created 或 destroyed
- energy 只能轉換其形式,或是只能從一個 object 傳遞到另一個
舉幾個日常生活中的例子 :
- 燈泡將 electrical energy 轉換成 light energy (radiant energy)
- 撞球撞到下一顆球,傳遞 kinetic energy
- 植物將陽光 (radiant energy) 轉換成 chemical energy 並儲存起來
- 你將吃的東西 (chemical energy) 轉換成你的任何動作、呼吸 (kinetic energy)
這些 energy 的轉換並不是非常的有效率
- 一開始的 energy 可能在途中被釋放出一些 thermal energy,也就是 HEAT
- 在燈泡上顯而易見,因為除了產生光以外燈泡也會產生熱
- 撞球摩擦撞球桌 (friction),也會產生熱
- 這些 heat generation 也非常重要,跟第二個法則有關
The Second Law of Thermodynamics
所以根據第一個法則,能量可以無限循環利用對嗎 ? (嗯... 對但不對)
- Energy 雖然不能被 created 或 destroyed
- 但 energy 可以從 more-useful form 轉換成 less-useful form
- 事實上,目前知道的所有 energy transfer 都是這種模式
- 轉換成的 less-useful 根本是 unusable energy
- 而這些 unusable energy 通常就是以 heat 形式出現
Heat 在正確的環境下使用不是可以做功嗎 ?
- 是的,但 heat 永遠無法 100% 轉換成其他 useful energy
- 所以每當 energy transfer 發生
- 一些 useful energy 就會被永遠轉換成 useless energy
Heat and Universe
這些沒用的 heat 最終會增加宇宙的 randomness (disorder) !
- 舉例來說,你有兩個不同溫度的 metal 放在一起
- 在冷金屬的 molecules 會移動較慢,另一邊熱金屬的移動較快 (ordered)
- 當 heat 自動要從熱傳遞到冷的一方時
- 熱金屬的 molecules 移動變慢,相反的冷金屬的 molecules 則移動變快
- 這個情況會持續到兩邊的 molecules 移動的平均速度都差不多 (disordered)
- 所有的 system 都會趨向從 ordered 狀態一路變成 disordered
- 因為 disordered 提供較多的新狀態可以選擇
Entropy
System 的 degree of randomness (或 disordered) 會以 entropy 來表示 !
Second Law of Thermodynamics
現在我們已經知道 energy 一定會從 useful 轉換到 unusable form (e.g., heat), 我們可以定義 biology-relevant 的 second law of thermodynamics
- 每個 energy transfer 會增加宇宙的 entropy (減少可以做功的 energy)
- 更精確地講,任何 chemical reaction 或一組 connected reactions 都會增加宇宙整體的 entropy
總結一下 :
- First Law 告訴我們 processes 中 energy 的 conservation
- Second Law 告訴我們 processes 的 directionality
- from lower to higher entropy (in overall universe)
Biological System
Second law of thermodynamics 告訴我們任何的 process 都會增加宇宙的 entropy,所以我們來實際看看一個人的活動影響了那些事
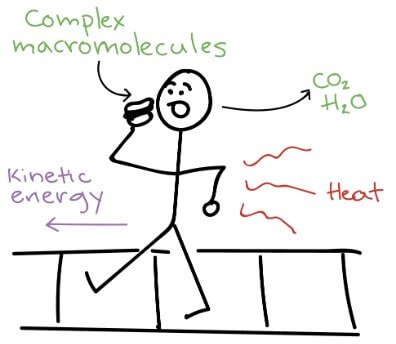
- 走路時肌肉收縮,讓腳可以移動身體前進
- 這是用了大量 molecules 中的 chemical energy (e.g., glucose) 來產生 kinetic energy
- 這個行為其實非常 low efficiency,也就是會產生非常多的 unusable energy (heat)
- 一些 heat 會讓身體暖起來,但很多 heat 會消散在周圍環境
- Heat 消散在周圍環境,代表讓周圍的 entropy 增加
- 呼吸時將很多簡單的 molecules (e.g., carbon dioxide, water) 透過 metabolize 吸收成走路的燃料
- 這些分解 molecules 的動作一樣釋放了 heat,一樣增加了 surroundings 的 entropy
- 雖然有一些 processes 能 locally decrease entropy
- 例如 build, maintain 較高等級的身體元件
- 但它們需要花費更多的 energy,這些 energy 也會消散成 unusable form
- 總體而言,local decrease entropy process 和 energy transfer 兩者 Overall 是增加了宇宙的 entropy
Free Energy
- 這邊的 free energy 指的不是免費的能源
- free energy 是用來測量 chemical reaction 造成多少 usable energy 的釋放 (消耗)
- 一個 process 若要自發性的發生
- 那一定是沒有 input 任何 energy
- 就讓 universe 的 entropy 增加
Gibbs free energy (G) 可以測量 process 是否自發性發生 :
測量時必須在一定的 temperature, pressure,而生物的系統正好符合
ΔG 是 gibbs free energy 的變化
- 若是大於 0,代表 process 非自發性發生
- 若是小於 0,代表 process 是自發性發生
ΔH 是 enthalpy 的變化
- 在 biology 中 enthalpy 代表儲存在 bonds 的 energy
- 所以 change of enthalpy 代表最終 products 和最初 reactants 的 bond energy 差異
- 若是大於 0,代表 reactants 到 products 的途中沒有 heat 被釋放 (因為能量變多)
- 若是小於 0,代表 reactants 到 products 的途中有 heat 被釋放 (因為能量變少)
ΔS 是 entropy 的變化
- 若是大於 0,代表 system 在 reaction 後變得更加 disordered
- 例如 large molecules 被拆成更多 small molecules
- 若是小於 0,代表 system 在 reaction 後變得更加 ordered
- ΔS 必須再和溫度 (T) 相乘,得到實際 ∆S 的影響
- 若是大於 0,代表 system 在 reaction 後變得更加 disordered
ΔG 是負的,代表不需要 input energy 就可以進行
- Spontaneous
相反的話,就需要 input energy 才能進行
- Non-spontaneous
以下整理了 ΔS 和 ΔH 的所有可能性
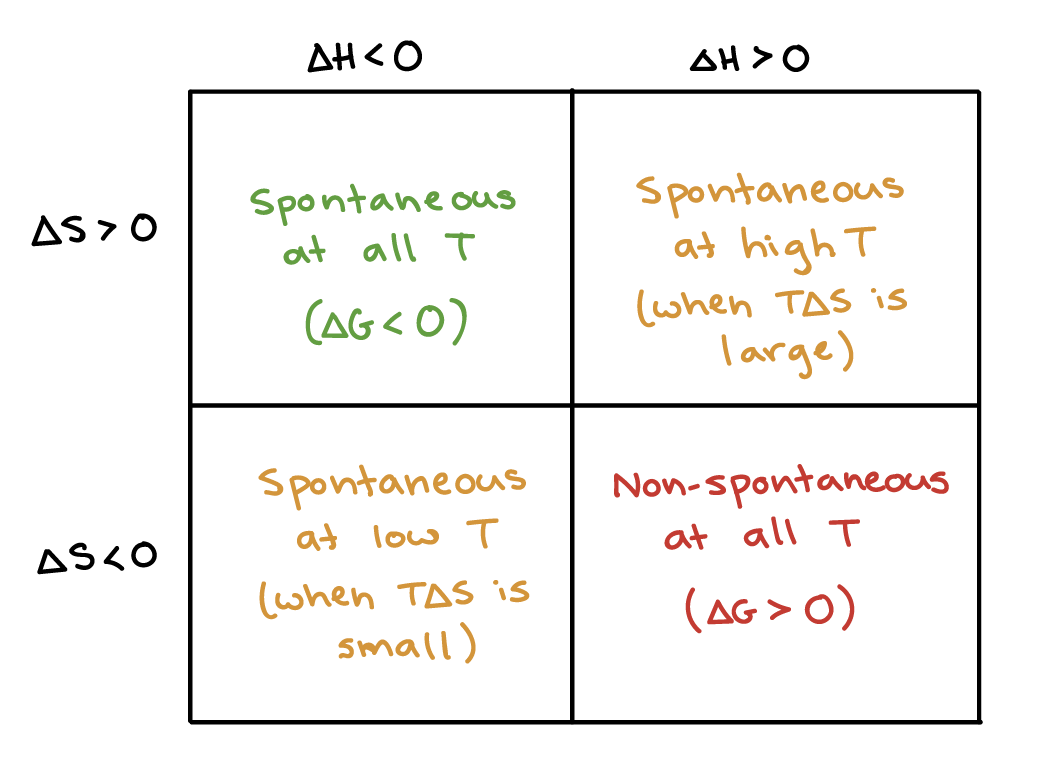
- 總結,若 reaction 釋放 heat (ΔH < 0) 且增加 entropy (ΔS > 0)
- 那 reaction 不管什麼溫度,都會是 spontaneous
- 若 reaction 沒有釋放 heat,又沒有增加 entropy
- 那 reaction 不管什麼溫度,都會是 non-spontaneous
- 其他的 reaction 則要依照溫度來判斷
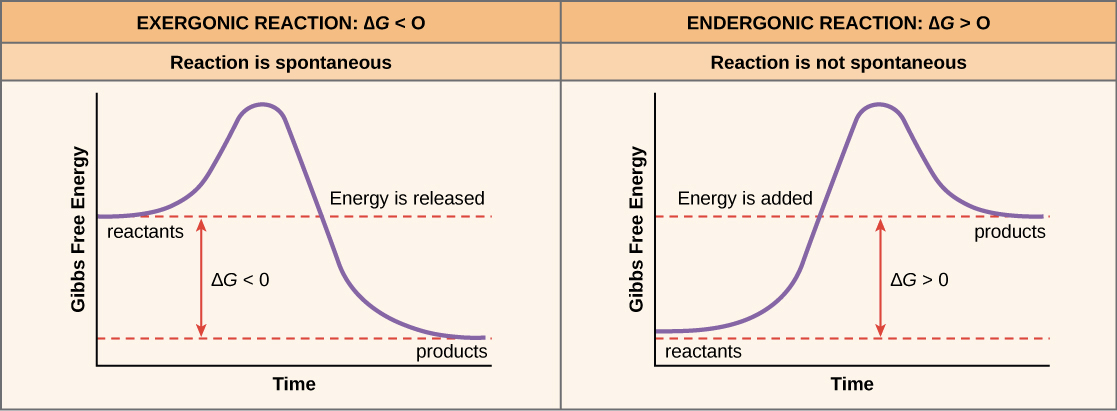
Endergonic and exergonic reactions
exergonic reactions (spontaneous)
- 指的是 ΔG 為負的,釋放 free energy 的 reactions
- Reactants (initial state) 比 products (final) 還要更多 free energy
endergonic reactions (non-spontaneous)
- 指的是 ΔG 為正的,需要 input energy 的 reactions
- Product 反而比 reactants 的 free energy 還要多
- 所以一定需要外部提供 energy 才能進行反應
ATP and reaction coupling
- 細胞中那些 endergonic reactions 需要 input energy
- 這些 energetically unfavorable reactions 跟 energetically favorable reactions "購買"其所釋放的 energy
- 購買的 energy 會是一種小分子,稱作 adenosine triphosphate, ATP
ATP structure and hydrolysis
- Adenosine triphosphate, ATP 可以視為 cells 的 energy currency
- energy 將會儲存在 ATP 中
- 需要使用時,透過 hydrolysis 將 ATP 分解成需要的 energy
- 下圖是一個 ATP 的完整架構
atp_structure
- ATP 就是 RNA 中 adenine based 的 nucleotide
- 而從 ribose 近到遠的三個 phosphate group 分別為 alpha, beta, gamma
- ATP 就是因為這三個 group 中含有負電的 phosphate tail 所以 unstable
- 意思是這三個 phosphate 都彼此想要和對方分開
- 這三個 phosphate 的 bonds 又稱作 phosphoanhydride bonds
Hydrolysis
- 因為 phosphoanhydride bonds 透過 hydrolysis 斷開時會釋放大量的 energy
- 所以又稱作 high-energy bonds
- 以下是 ATP 透過 hydrolyze 變成 ADP 的模樣
其中的 P 指的是被分開的那個 inorganic phosphate group
- ATP 到 ADP 的反應是可逆的,需要加入新的 energy 才可以進行逆反應
- 重新生成 ATP 對細胞來說是相當重要的
- 因為細胞會很快的分解完所有 ATP 拿到 energy,所以要馬上再組合回 ATP
- 你可以想像拿著 ATP 的細胞就是充飽電的情況
- 當電池沒電,就要分解成 ADP 充電

- ATP 透過 hydrolysis 分解後到底能拿到多少 energy 呢
- 在一般情況下 ATP to ADP 產生的 ∆G 為
- 而在細胞中可以達到兩倍 :
Reaction coupling
- ATP 轉 ADP 被釋放的能量細胞將透過 reaction coupling 來使用
- ATP hydrolysis 這個 exergonic reaction 將會連結到 endergonic reaction
- 兩個 reaction 的 link 稱作 shared intermediate
- 第一個 reaction 的 product 會作為第二個 reaction 的 reactant
這樣把兩個 reaction 合起來有什麼好處嗎 ?
- 若 exergonic 的 ΔG 比 endergonic 的 ΔG 還要負更多的話
- 這兩個反應合起來就會是一個 ΔG 為負的 exergonic reaction
- 也就是讓 endergonic 也變得能夠自發性發生了 !
- 實際上 shared intermediate 可以看成以下的簡單加法
- B 看起來消失了,但這其實表示著他成為兩個式子的 product 和 reactant
- 所以兩個 B 彼此被 cancel out
ATP in reaction coupling
若 reaction coupling 包含 ATP 的時候, shared intermediate 通常會是 phosphorylated molecule, 以下用合成 sucrose 作為範例 :
- 要合成 sucrose 需要 energy,所以是 endergonic reaction (不是自發性的)
- ΔG 是 +27 kJ/mol
- 我們可以將 ATP hydrolysis 這個 exergonic 加入進來幫忙"支付" energy
- ΔG 是 -30 kJ/mol
- ATP hydrolysis 所產生的 energy 是怎麼幫助 sucrose 合成的,其實不只一個 reaction 就解決
- 第一個 reaction 中,ATP 的 phosphate group 跑到 glucose
- phosphate 跟 glucose 在一起變成 phosphorylated glucose (glucose-P)
- 這個 reaction 就是一個 energetically favorable 的 reaction
- 因為 ATP 是 unstable 的,非常想要把他的 phosphate group 給別人
- 第二個 reaction 中,glucose-P 就會跟 fructose 一起合成 sucrose
- 因為 glucose 現在有 phosphate,所以他也變成 unstable
- 所以這個 reaction 一樣會釋放 energy,然後也是 spontaneous
- 第一個 reaction 中,ATP 的 phosphate group 跑到 glucose

以上這個方法,大量使用在細胞中的 metabolic pathways, 利用 ATP to ADP 產生的 energy 來推動各種 reactions
Activation energy
你今天有非常多的事情要做,你感到很有幹勁,但你必須要先起床,而起床又是一個難關 (hump)
- Reaction 在進行前也需要先經過一道 energy hump
- 這個 hump 稱作 activation energy
- 連 exergonic reaction 一樣需要先突破 activation energy 才能開始
- activation energy 的簡寫是
為什麼連 exergonic (energy-releasing) reaction 這種負 ∆G 的反應都需要先有 energy 才能執行呢 ?
- Reactants 要變成 products 之前,需要先把 bonds 都先打掉重用
- 為了把 bond 都打掉,molecules 必須先變成 unstable state
- 也就是 molecules 必須把自己 contort (deform, bent) 起來
- 這個 state 稱為 transition state
- 因為 transition state 是一個非常高 energy 的 state
- 所以必須有 activation energy 的加入才能達到
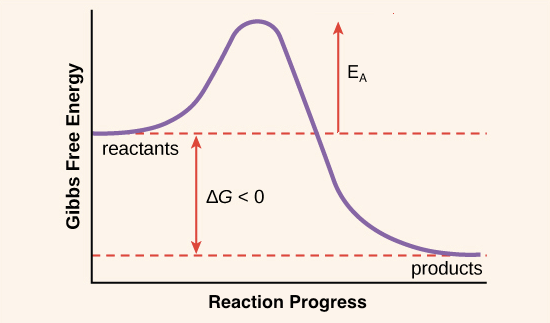
- Activation energy 的來源通常是 heat
- 這些 heat 由 reactant molecules 從周遭吸收而來
Reaction Rate
- Activation energy 的量會和 reaction 的速率呈現對比
- energy 的需求越高,那麼 reaction 就會越慢
- 在有些情況下是好事 (e.g., propane),但有些情況需要加速,該怎麼加速
- 幫助減少 activation energy 加速 reaction 的動作稱為 catalysis
- 實際影響這件事的 factor 稱為 catalyst
- 而在生物界的 catalyst 就是 enzymes
Enzymes
- Enzymes 通常為 proteins,有一些 RNA molecules 也會進行 enzyme 的行為
- 跟前一章節講得一樣,enzymes 會幫助降低 activation energy
- 加速 chemical bond-breaking & bond-forming processes
例如下圖紫線是 enzymes 尚未幫忙的狀況,綠線就是 enzymes 加入後的狀況
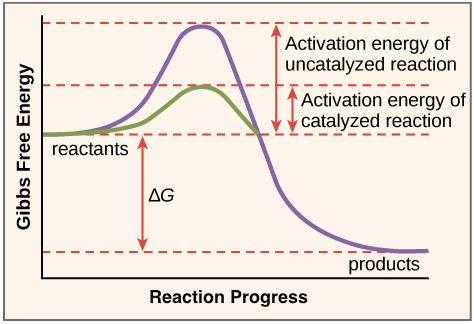
- 注意的是,enzymes 只會幫助降低 transition state 的 energy
- Enzymes 並不會改變 ∆G,也就是不會改變 reaction 的本質 (exergonic or endergonic)
Active sites and substrate specificity
在 catalyze 時,Enzyme 會抓取需要被幫助的 reactant molecules (1 or more)
- 這些被幫忙的 molecules 稱為 substrates
- 有的單個 substrate 可以被拆分成多個 products
- 有的兩個 substrates 合併成一大個 products 或是被互換一些東西
- 幾乎所有的 biological reaction 都有 enzymes 在加速
- 這些被幫忙的 molecules 稱為 substrates
Enzyme 和這些 substrates 互相 bind 在一起的地方稱為 active site
- 還記得 protein 是由 amino acids 組合而成的
- 所以 active site 擁有各種 amino acids 獨一無二的 properties
- 這讓不同 enzyme 的 active site 能夠獨特的和一些 substrate 一起運作

- 另外,除了 amino acids 的特徵會改變 active site 以外,環境也是很重要的因素
- Temperature
- 不管升高 temperature 或降低 temperature 都可能造成 enzyme 暫停或中止
- pH
- 過高或過低的 pH 跟溫度一樣,最極端會造成 enzyme 被 denature
- Temperature
Induced fit
- Enzyme's active site 和 substrate 並非像拼圖一樣 (lock-and-key model)
- Enzyme 會在 bind substrate 的時候些微的改變自己形狀
- 這個行為稱為 induced fit

對了,enzymes 到底怎麼樣讓 activation energy 降低的 ?
- 這其實是根據 enzyme 不同有不同的做法
- 有的將 substrates 以正確的 orientation 合併
- 有的將 active site 布置成適合 reaction 的環境 (acidic, nonpolar)
- 有的將 substrate 的架構弄得更容易分解,更容易達到 transition state
有一點重要的事是 enzyme 不會受到 reaction 影響
- Enzyme 最終會回歸原本的狀態
- Enzyme 釋放 product 後可以馬上進行下一個 catalysis
Enzyme regulation
Enzymes 為了協助細胞的 metabolism,必須要被更小心的控制,以下是幾個常見會影響 enzyme activity 的因子
- Regulatory molecules
- bind 在 enzyme 上的 activator, inhibitor molecules 有時會控制 enzyme activity
- Cofactors
- 有時 enzyme 還需要額外的 non-protein helper molecules 來幫忙運作
- Compartmentalization
- 儲存時正確的分隔 enzymes 能有效避免造成傷害或提供正確環境來運作
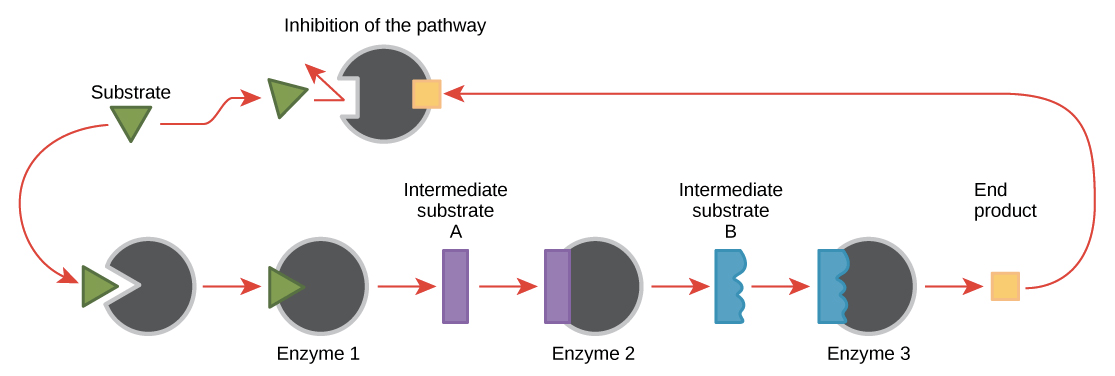
- Feedback inhibition
- 關鍵的 metabolic enzymes 往往會被最終 product 限制住
Regulatory molecules
- Enzymes 會受到其他 molecules 影響,增加或減少 activity
- 讓 activity 增加的 molecules 稱為 activators
- 讓 activity 減少的 molecules 稱為 inhibitors
多數的 activator, inhibitor 都是 reversible 的, 不會永遠和 enzyme 互動
- 例如一些重要的藥就是 reversible inhibitors
- tipranivir (treat HIV)
- 防止 viral enzyme 幫助 virus 複製
Reversible inhibitors 可以有非常多種類,下面講兩個重要的 group
- competitive inhibitors
- noncompetitive inhibitors
Competitive vs. noncompetitive
- Competitive inhibition
- inhibitor 會跟 substrate 搶奪 enzyme 的 active site
- 先到先贏,後到就不能和 active site 綁定起來
- Noncompetitive inhibition
- inhibitor 會到別的地方 (another site) 和 enzyme 綁定
- substrate 也可到 active site 綁定
- 但 inhibitor 的綁定會讓整個 enzyme 無法正常運作

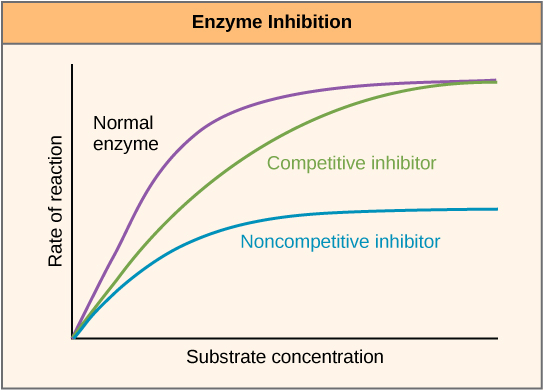
- 當 inhibitor 是 competitive 的時候
- 若 substrate 數量很少
- Reaction rate 會降低
- 若 substrate 數量很多
- 幾乎所有的 enzymes 的 reaction rate 一樣可以達到 maximum
- 因為 inhibitor 搶不贏阿
- 若 substrate 數量很少
- 當 inhibitor 是 noncompetitive 的時候
- 不管 substrate 的數量多寡
- 所有的 reaction rate 都會降低
- 因為 inhibitor 就像"毒"一樣防止 enzyme 運作
- 不管 substrate 的數量多寡
Allosteric regulation
- 上面說的 noncompetitive inhibitor 會到不是 active site 的別的地方跟 enzyme 綁定
- 這些 activator, inhibitor 綁定的"別的地方"稱為 allosteric site
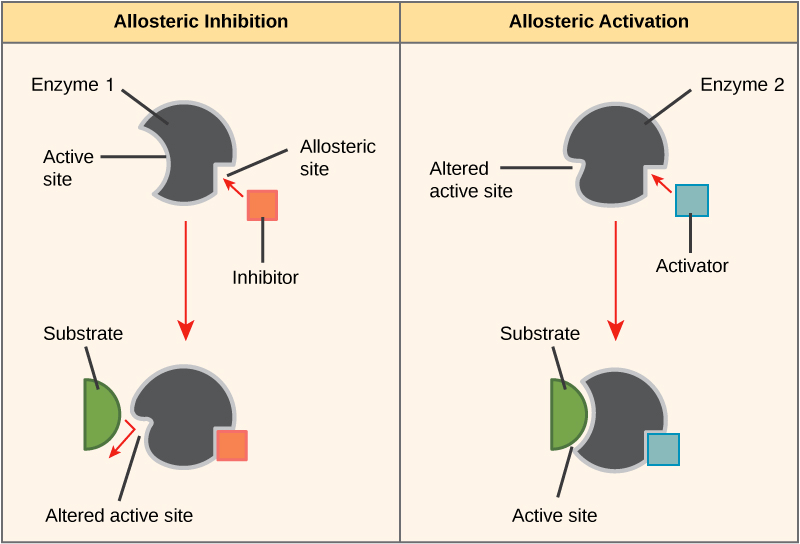
有些特別能夠接受 allosterically regulated 的 enzymes 會有特別的 properties
- 能夠 allosterically regulated 的稱為 allosteric enzymes
- 他們會有多個 active sites 分布在不同的 protein subunits 上
- 當 allosteric inhibitor 綁定在該 enzyme 時
- 所有的 active sites 都會變化,使得工作無法順利進行
- 當 allosteric activator 綁定在該 enzyme 時
- 所有的 active sites 的效能都可以變好
另外再 allosteric enzymes 上還會有 cooperativity 的行為出現
- 某些 substrate 可以作為 allosteric activator 的角色
- 當該 substrate 綁定到某個 active site 時
- 其他的 active sites 的效能也都會變好
Cofactors and coenzymes
有些 enzyme 無法自己就做到最好,需要其他 non-protein molecules 的幫忙
- 這些 non-protein molecules 稱做 cofactors
- 可能透過 ionic, hydrogen bonds 暫時綁定在 enzyme 上
- 可能透過強力的 covalent bonds 永遠綁定在 enzyme 上
- 舉幾個常見的 inorganic ions 的 cofactors
- iron
- magnesium
- 一些幫助建立 DNA 的 enzyme 就需要 magnesium ions 的幫助
Cofactor 還有一些子集合是 organic molecules (carbon-based)
- 這些 organic molecules 稱做 coenzymes
- 最常見的 coenzymes 是 dietary vitamins
- 有的 vitamins 是 coenzymes 的 precursor
- 有的 vitamins 本身就是 coenzymes
- 最常見的 coenzymes 是 dietary vitamins
例如 vitamin C 是非常多 enzymes 的 coenzyme
- 幫助建立 protein collagen
- Connective tissue 的重要元件
Enzyme compartmentalization
Enzymes 會被 compartmentalize,也就是儲存在 cell 的不同 part,執行各自的工作
例如在 organelle (細胞器官) 中
- enzymes 根據特定工作被分配在不同的位置
- 如此一下 enzymes 可以更快找到跟他相應的 substrates
- 也可以防止 enzyme 傷害到 cell
例如 lysosome 中的 digestive enzymes (lysosomal enzymes)
- 需要在 pH 為 5.0 的環境下才能工作
- 所以通常只能在 lysosome 的 acidic interior 才能找到他們
- 而不會在一般的 cytosol (pH 7.2) 看到他們
- 他們就像 cell 的 "insurance" 一樣
- 就算 lysosome 爆裂,這些 enzymes 也不會去傷害 cell (因為不能在 7.2 環境下運作)
Feedback inhibition of metabolic pathways
生成的 product 防止更多 product 被產出的 regulation 稱為 feedback inhibition
- 這是一個很好的方法讓 cell 產出剛好數量的 product