Macromolecules
Macromolecules 是一種大分子,通常由很多小單位重複的組成,這些小單位叫作 monomers。這些 macromolecules 大多是用 dehydration synthesis reactions 來組合而成,而有時會需要 hydrolysis reaction 來拆解。常見的 macromolecules 包括 carbohydrates、lipids、nucleic acids 和 proteins,且每個 macromolecule 都有提供不同功能的特性與結構。
Introduction
- 人類是由一堆 large biological molecules 組合而成
- 更可以將人類看成由 4 major types of large biological molecules 組成
- carbohydrates (such as sugars)
- lipids (such as fats)
- proteins
- nucleic acids (such as DNA and RNA)
- 這些 large biological molecules 在生物中處理非常多的工作
- carbohydrates : store fuel, energy
- lipids : key structure components of cell membranes
- nucleic acids : store, transfer hereditary information (instruction for making proteins)
- proteins : 最多功能性
- structural support
- carry out specific jobs in a cell, such as catalyzing metabolic reactions, receive or transfer signals
Monomers and polymers
- 這些大多數的 large biological molecules 都是 polymers (視為 necklaces, series of beads)
- Polymers 又是由很多小單位重複的組成,這些小單位叫作 monomers (視為 beads)
- Carbohydrates, nucleic acids, proteins 這三類通常在自然中為 long polymers
- 這三種又會被稱作 macromolecules (marco- : big, large, huge)
- Lipids 則是四個裡面最小的,甚至不會是一個 polymer
- 有的時候 lipids 不會被考慮在 macromolecules 中
- 但很多時候還是會稱這四個 large biological molecules 為 "macromolecule" (more loosely)
備註
只要記得 lipids 也是 large biological molecules 的一員,但只是他不常形成 polymers
Dehydration synthesis
- 這些 large biological molecules 通常透過 dehydration synthesis reaction 聚集起來
- 也就是 monomers 之間會透過 covalent bond 起來,且過程中會釋放水分子
- 這也是為什麼叫作 dehydration
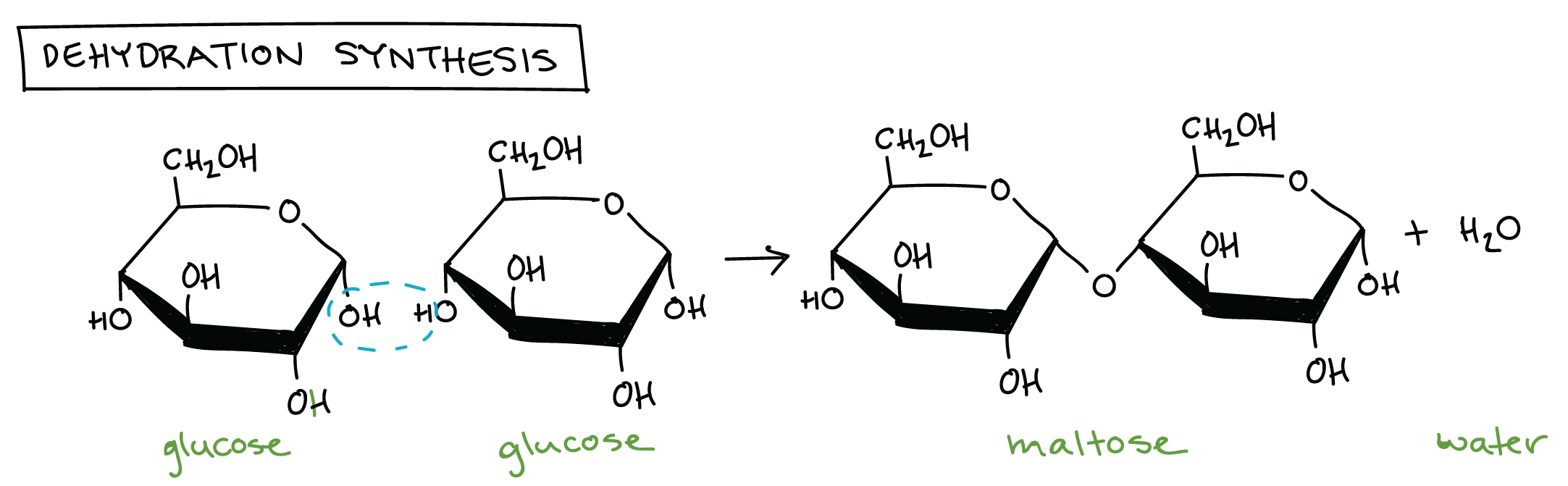
- 例如上圖的 dehydration synthesis reaction
- 可以看到 2 個 sugar glucose 組合成 1 個 sugar maltose + 水分子
- 其中一個 glucose 損失一個 H,另一個損失一個 OH group
- 失去的兩個東西 (H 和 OH) 用 covalent bond 的形式組合成水分子
- 其他的 monomers 也用這個方式合成,最後就形成越來越長的 polymer
- polymers 雖然單純重複 monomer 組成,但可以有非常多的 shape, composition
- composition, sequence 的不同會影響 function
- carbohydrates, nucleic acids, proteins 都能有非常多不同類型的 monomers
- 例如 DNA 有 4 種 nucleotide monomers
- proteins 有 20 種 amino acid monomers
- 單一種類的 monomer 也可以組成不同的 polymers (當然就擁有不同 properties)
- 例如 starch, glycogen, cellulose 都是由 glucose monomers 組成的 carbohydrates
- 但都有不同的 bonding 和 branching patterns
Hydrolysis
- polymers 有時需要被轉換回 monomers
- 例如身體會回收 molecule 來重新 build 其他的 molecule
- polymers 會透過 hydrolysis reaction 來分解成 monomers
- 也就是原本組合 monomers 的 bond 會被水分子斷開
- 在 hydrolysis reaction 當中,原本的組成分子會被一分為二
- 其中一個 molecule 得到 hydrogen atom
- 另一個 molecule 則得到 hydroxyl group
- H 和 -OH 兩者都是從 dehydration synthesis 產生的水分子而來
- 所以 hydrolysis 其實就是 dehydration synthesis 的逆反應
- 這些被轉換回的 monomer 可以重組成新的 polymer
- 例如下圖中水分子把 maltose 拆成 2 個 glucose monomers
- 這是原先上圖那個 dehydration synthesis 的 reverse
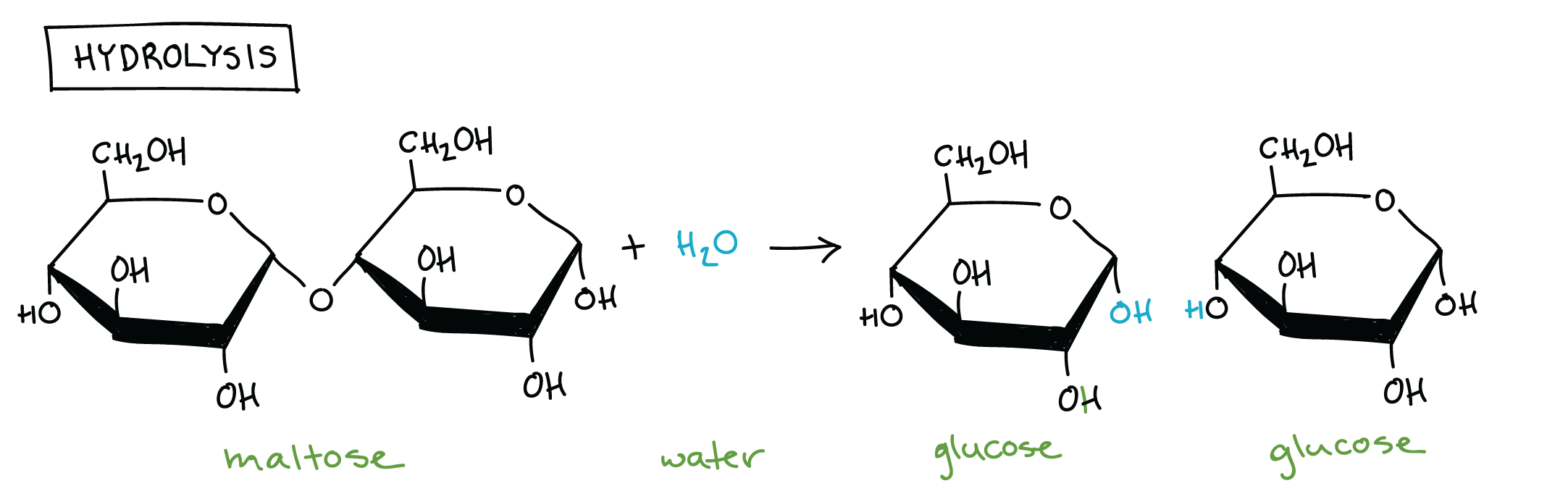
- Dehydration synthesis reactions 需要能量來組合 molecules
- Hydrolysis reactions 則是把 molecules 拆解並釋放能量
- Carbohydrates, proteins, nucleic acids 就是透過這些 reactions 不斷建立又拆解,儘管他們的 monomers 都是不同的
備註
- 在 cell 中的 nucleic acids 實際是不會用 dehydration synthesis 來合成
- 有些種類的 lipids 也會使用 dehydration synthesis 來合成,儘管 lipids 不是 polymers
Enzymes
- 身體中的 enzymes 通常會加速 (catalyze) dehydration synthesis 和 hydrolysis 兩種反應
- 而破壞 bond 的 enzymes 通常命名的結尾會有 -ase
- 例如 maltase enzyme 用來分解 maltose
- lipases 用來分解 lipids
- peptidases 用來分解 proteins
- enzymes 可以分解任何 large biological molecules
- 將物質釋放成 small building blocks 供身體吸收及使用
Carbohydrates
- 一些 carbohydrates 以 sugar 型態現身,提供吃的人 fuel source
- 一些 carbohydrates 則是 fiber 型態,例如 cellulose polymers 提供細胞壁結構
- 大多 carbohydrates 是 starch 型態,是一連串連結的 glucose molecules (儲存能量)
- 當吃下薯條時,我們消化道的 enzymes 就是在這串 glucose 上將他們切斷成一個一個的 sugar,讓 cell 可以使用
Monosaccharides
- monosaccharide (mono- = one, sacchar- = sugar) 是單醣
- 最常見的是 glucose
- formula 是 ,通常有 3 到 7 個 carbon atoms
- monosaccharide 中的 oxygen atom 會出現在兩個地方
- hydroxyl group
- carbonyl group,這個 group 的位置會改變糖的種類
- 若 carbonyl 包在 aldehyde group (在最後 chain),那這個糖就是 aldose (醛糖)
- 若 carbonyl 被包在兩個 C 中間 (不在最後 chain),就會形成 ketone group,而成為 ketose (酮糖)
- 另外糖的名字還可以依照 carbon 數量命名,例如 trioses (3 carbons)、pentoses (5 carbons)、hexoses (6 carbons)
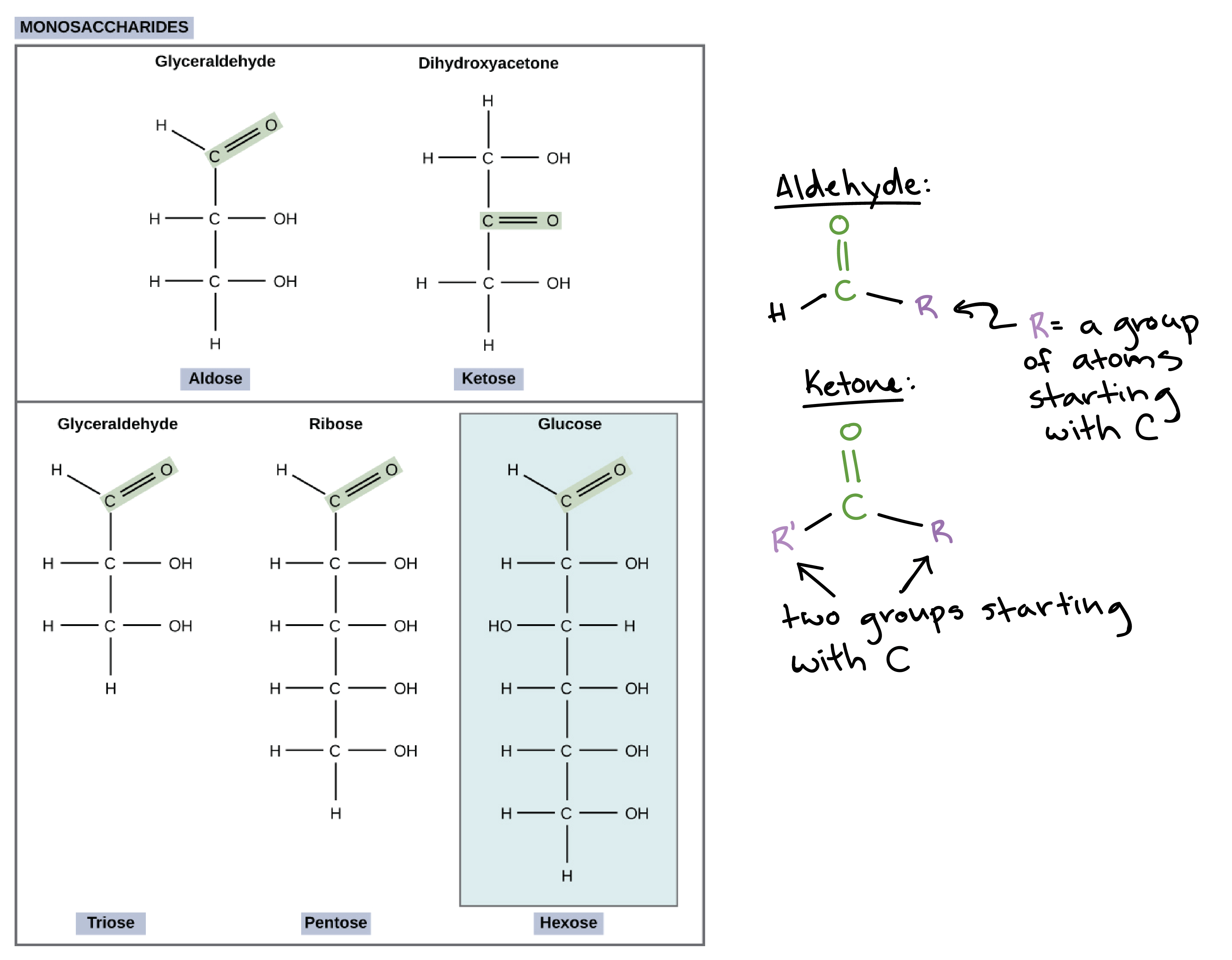
Glucose
- glucose 是 monosaccharide 重要的一員,有 6 個 carbon 寫作
- 另外常見的 monosaccharides 還有 galactose (半乳糖), fructose (果糖)
- 但它們三個的 formula 都一模一樣 ()
- 所以他們是 isomers
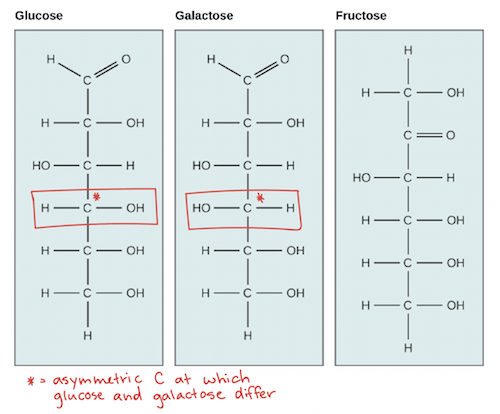
- Fructose 和 glucose 是 structural isomer
- Galactose 和 glucose 則是 stereoisomers
- 這些小細節都足夠告訴 enzymes 來取得正確要使用的糖來進行 chemical reactions
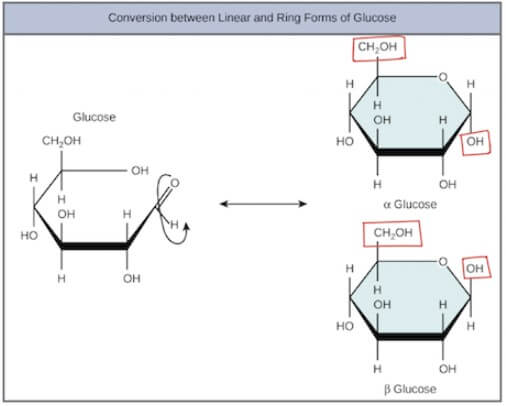
Ring forms of sugars
- 除了上面三種 linear chain 的糖,其他還有很多 ring-shaped 的糖
- 有些 5, 6 carbons 的糖可以存在 linear 以及 ring-shaped
- 這些型態都能達到 equilibrium,但 ring 才是最好達到的型態 (特別是在水中)
- glucose 有 99% 都是以 6 carbon ring form 存在 solution 中
- Glucose 在 6 個 carbon ring 還會有兩種型態
- alpha form
- 當 carbonyl 轉成 hydroxyl group 在 ring 之上時 (跟 同邊)
- beta form
- 同樣當 carbonyl 轉成 hydroxyl 並在 ring 之下時
- alpha form
Disaccharides
- disaccharide (di- = two) 是雙醣
- 是兩個 monosaccharides 透過 dehydration synthesis (condensation reaction) 結合在一起的
- 其中一邊的 hydroxyl group 和另一邊的 hydrogen 結合
- 釋放出水分子後形成了 glycosidic linkage (covalent bond)
- 例如下方是一個 glucose 和 fructose 兩個 monomers 組合的情況
- 透過 dehydration 形成 sucrose (table sugar,蔗糖)
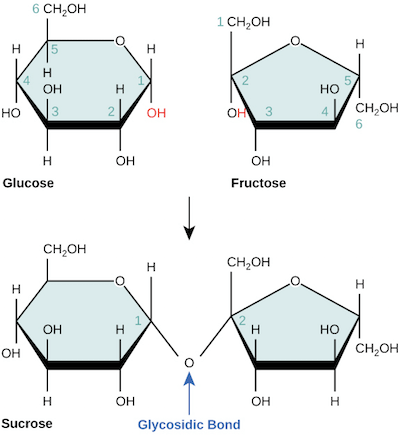
- 結合時 monosaccharide 中 carbon 的位置非常重要
- 我們從離 carbonyl group 最近的 carbon 開始從 1 標號碼
- 可以看到 glucose 的 1 carbon 和 fructose 的 2 carbon 連結在一起
- 這個 bond 就是一個 1-2 glycosidic linkage
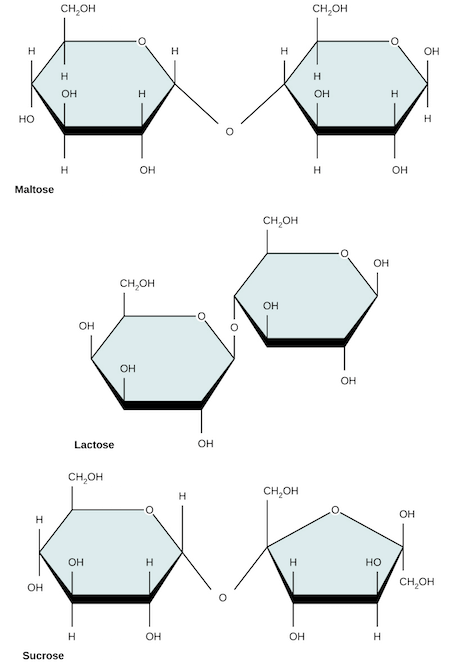
- 常見的 disaccharide 有 lactose (乳糖), maltose (麥芽糖), sucrose (蔗糖)
- lactose = glucose + galactose
- maltose = 2 * glucose
- sucrose = glucose + fructose
Polysaccharides
- 大量的 monosaccharides 透過 glycosidic bond 連結起來就是 polysaccharides (多醣)
- chain 可以是 branched 或是 unbranched
- 可以包含各種類型的 monosaccharides
- 常見的 polysaccharides 有
- Starch (澱粉), glycogen (肝糖), cellulose (纖維素), chitin (甲殼素)
- 都是對生物非常重要的多醣
Storage polysaccharides
Plants
- Starch 是植物中糖的 stored form
- 由 2 個 polysaccharides (amylose + amylopectin) 組成
- 2 個都是由 glucose 組成的 polymers
- 植物透過光合作用產生大量的 glucose 來維生
- 還沒使用到的 glucose 就會轉成 starch 形式儲存在 roots 或 seeds
- 在 seed 中的 starch 提供胚胎養分,或是成為動物的食物
- 動物再透過 digestive enzymes 來分解 starch 成為 glucose monomers 吸收
- 還沒使用到的 glucose 就會轉成 starch 形式儲存在 roots 或 seeds
- 由 2 個 polysaccharides (amylose + amylopectin) 組成
- 在 starch 中,glocose monomers 都是 alpha form
- hydroxyl group of carbon 1 sticking down below the ring
- 而且 connect 的方式多為 1-4 glycosidic linkage
- 舉例來說
- Amylose 由 linear chain 的 glucose 組成,連接方式是 1-4 glycosidic linkage
- Amylopectin 是 branched polysaccharide,連接方式大部分是 1-4 glycosidic linkage,有一些是 1-6 linkage 在 branch 處
- 舉例來說
Humans
- Glycogen 是人類中糖的 stored form
- 跟植物一樣,也是由 glucose monomers 組成的 polymer
- 甚至比 amylopectin 還要多 branches
- 通常 glycogen 儲存於 liver, muscle cells
- 當血液中的 glucose level 下降
- glycogen 就會透過 hydrolysis 分解,然後釋放 glucose 到血液中
- 當血液中的 glucose level 下降
Structural polysaccharides
- polysaccharides 除了當作能量來源,另一個重要用途就是作為 structure
- 例如 Cellulose 用於植物的 cell walls,負責包圍細胞
- 樹和紙都是由 cellulose 組成
- cellulose 由大量的 glucose monomers 透過 unbranched chains 由 1-4 glycosidic bonds 組成
- 例如 Cellulose 用於植物的 cell walls,負責包圍細胞
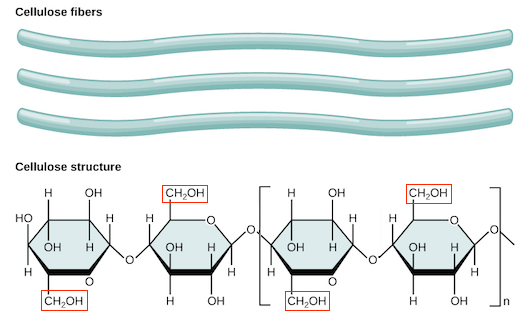
- cellulose 中的 glucose 則是 beta form
- 可以看到上圖每一個 glucose 都和鄰居成上下顛倒的情況
- 這讓 cellulose 的形狀是 long, straight, non-helical chains
- 這些 chain clusters 中每個的 hydroxyl group 再透過 hydrogen bonds 連結
- 所有的特性讓 cellulose 非常 rigid,且有高度 tensile,適合作為細胞壁
- cellulose 中的 beta glycosidic linkages 是人類的 digestive enzymes 所無法分解的東西 (所以人類無法消化 cellulose)
- 但是有一些草食動物,例如 cow, koala, buffalo, horse
- 體內有一些特別的 microbes 幫助他們處理 cellulose
- 這些 microbes 生存在動物的消化道,把 cellulose 分解成 glucose monomers 供動物使用
Chitin
- 某些昆蟲有 hard external skeleton 稱作 exoskeleton (外骨骼)
- 是為了保護他們較脆弱的內部身體而存在
- 這些 exoskeleton 由 macromolecule chitin 組成
- 結構跟 cellulose 很像,但是 glucose 和 nitrogen-contained 的 functional group 組合在一起
Lipids
- 我們都以為 fat 是對身體很不好的東西,但實際上是生物中非常重要的角色
- 近年的研究甚至發現 sugar 可能比 fat 帶來更多的健康問題
- Fat 由 1 個衣架形狀的 molecule 稱作 glycerol (丙三醇又稱甘油)
- 和 3 個 long hydrocarbon tails (fatty acids,脂肪酸) 組合在一起
- Fats 只是 Lipid 的一種
- 因為 lipids 多由 hydrocarbon chains 所組成,所以是特別不會溶於水的 molecules (hydrophobic, nonpolar)
- Lipids 可以有多種功用,例如 :
- store energy (long-term)
- insulation (cell membranes)
- water-repellent (on leaves)
- building blocks for hormones (testosterone)
- 甚至有很多維他命是 fat-soluble,表示他們只能跟 fat molecules 作用,才被人體吸收
- 以下我們先針對幾種常見的 lipids 來介紹
- fats, oils, waxes, phospholipids (磷脂), steroids (類固醇)
Fats and Oils
- Fat molecule 包含兩大部分
- glycerol backbone
- 包含 3 個 hydroxyl (OH) groups
- three fatty acid tails
- 每個由 12 至 18 個 carbon 組成 hydrocarbon 分別連結至 hydroxyl group
- 還是有少如 4 個 carbon 或多如 36 個 carbon
- glycerol backbone
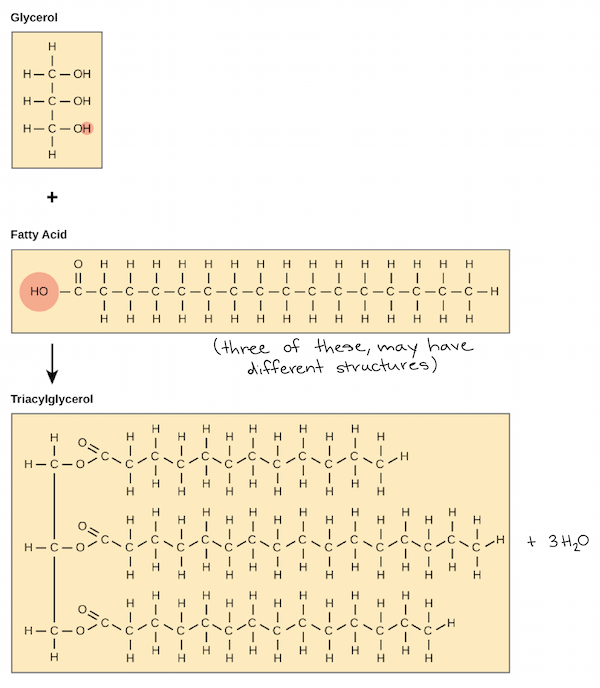
- glycerol 的 hydroxyl 將會與 fatty acids 的 carboxyl 進行 dehydration synthesis 合成
- 所以 glycerol backbone 會以 ester linkage 和 3 個 fatty acid tails 連結起來
- ester linkage : oxygen atom next to a carbonyl group
- 所形成的 fat molecules 可以稱作 triglycerides (三酸甘油酯)
- triglycerides 可能會有 3 個完全相同的 fatty acid tails
- 也可能會有 3 個完全不同的 fatty acid tails (diff length, diff patterns of double bonds)
- Triglycerides 又可以稱作 triacylglycerols
- Triglycerides 主要儲存於一些特別的 fat cells,稱作 adipocytes (脂肪細胞)
- adipocytes 會組成常見的 adipose tissue
- 有些不存在 fat 的 fatty acids 自己在人體中游移,這些也可當作 lipids
Saturated and unsaturated fatty acids
- 3 個 fatty acid chains 可以有不同的長度,而裡面的架構又會改變 degree of unsaturation
- 當 carbon 之間都是 single bond 的時候,這個 fatty acid 是 saturated 的
- 指的是跟 hydrogen 互相飽和 (saturated)
- 所有 hydrogen 都盡可能 attach 到 carbon skeleton
- 當 carbon 之間有出現 double bond 的時候,這個 fatty acid 就是 unsaturated 的
- 如果又只有一個 double bond,那就是 monounsaturated
- 如果有多個 double bond,那就是 polyunsaturated
- 這些 double bond 又可以有 cis 或 trans configuration
- Cis configuration
- Bond 兩邊的 hydrogens 在同一側
- 使得 fatty acid 產生 kink, bend
- Trans configuration
- Bond 兩邊的 hydrogens 在不同側
- 使得 fatty acid 是 linear
- Cis configuration
- 當 carbon 之間都是 single bond 的時候,這個 fatty acid 是 saturated 的
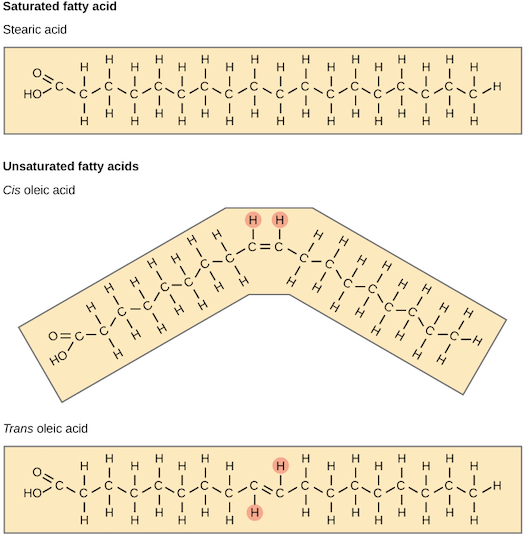
- Saturated fatty acid tails 是直的,所以該 fat molecules 能夠非常緊密的包在一起
- Pack tightly against one another
- 所以在室溫時會是固體 (high melting point)
- 例如一些 butter 就是 saturated fats
- Cis-unsaturated fatty acid tails 則是彎的,這讓 fat molecules 無法緊密包在一起
- 所以在室溫時會是液體 (low melting point)
- 例如一些常見的 oils 就是 cis-unsaturated fats
Trans fats
- 上面我們少講了 trans-unsaturated fatty acid tails (或稱 trans fat, 反式脂肪)
- Trans fats 在自然界非常稀有,但卻被工業中使用 partial hydrogenation 方式大量生產
- hydrogenation 意思是氫化,也就是灌入 hydrogen gas
- 通常會灌入 cis-unsaturated fats
- 試著讓那些 double bond 變回 single bond,也就是嘗試得到 saturated 的特性 (室溫固態)
- 但是卻出現一些副作用,例如 cis double bonds 變成 trans double bonds
- 常見的 trans fats 在室溫中是固體,例如大部分的 shortening, creamer
- Trans fats 在自然界非常稀有,但卻被工業中使用 partial hydrogenation 方式大量生產
- 看起來 partial hydrogenation 和 trans fat 表面上帶來的好處有
- 用 oil-like prices 就得到 butter-like substance
- 但實際上 trans fats 對人體有非常不好的影響
- 與 coronary heart disease 有非常大的正關聯性
Omega fatty acids
- omega-3, omega-6 fatty acids 也是值得一提的 fatty acids
- 這兩種 fatty acids 又有非常多種形態
- 但 omega-3 主要架構是 alpha-linolenic acid (ALA)
- 而 omega-6 主要架構是 linoleic acid (LA)
- 人體非常需要這兩種 fatty acids 但卻無法生成 ALA, LA 這兩種 essential fatty acids
- 只好從飲食取得,例如 fish (salmon), seeds (chia, flax)
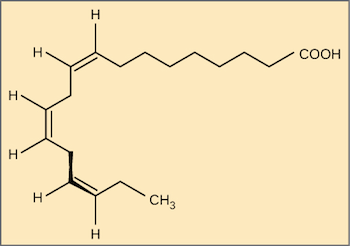
- omega fatty acids 都含有至少 2 個以上的 cis-unsaturated bonds
- 所以都是 curved 形狀,例如上圖的 ALA
- 這些 omega fatty acids 都扮演非常重要的角色
- 例如作為合成重要 signaling molecules 的 precursors
- 幫助調節 inflammation, mood
- Omega-3 fatty acids 減少 heart attack 這種瞬間死亡疾病的機率
- 或是減少血液中的 triglycerides、降低血壓、減少血栓形成
- 例如作為合成重要 signaling molecules 的 precursors
Waxes
- Waxes 是另一種重要的 lipids
- 常見在一些水棲鳥類的羽翼上、或是一些植物的葉面上
- Waxes 用了 lipid 中 hydrophobic (water-repelling) 的特性來防水
- Waxes 通常由 long fatty acid chains 和 alcohols 透過 ester linkages 組成
- ester linkage : oxygen atom next to a carbonyl group
Phospholipids
- 細胞中有 plasma membrane 來防止 cytosol (細胞液) 溢出
- 這些 plasma membrane 的主要成分就是 phospholipids (磷脂)
- phospholipids 組成方法跟 fat 非常像,只是他只有 2 個 fatty acid tails
- 而 glycerol backbone 的第三個 carbon 則跟 phosphate group 組成
- 這個 phosphate group 又可以有不同的 modifiers 得到不同的屬性
- 例如 choline (nitrogen-containing compound)
- 例如 serine (an amino acid)
- 這個 phosphate group 又可以有不同的 modifiers 得到不同的屬性
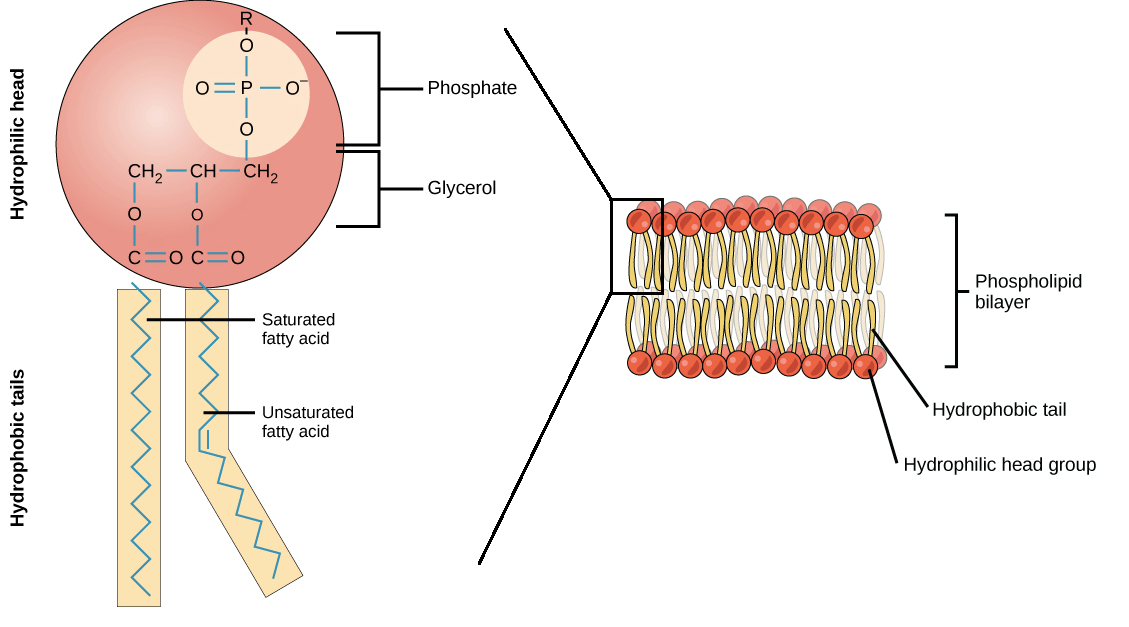
- phospholipids 是一種 amphipathic 的 molecule
- amphipathic 代表一半 hydrophobic 一半 hydrophilic
- phosphate 部分是 hydrophilic
- fatty acids 部分是 hydrophobic
- Membrane 的架構就是由 phospholipids 組成的 bilayer
- 其中 phosphate 面向水的一方,而 tails 則面向內部
- 這個架構讓 tails 不會碰到水,得到 low-energy, stable arrangement
備註
如果將 phospholipids 放到水中,會形成一個 sphere-shaped 的架構稱作 micelle >
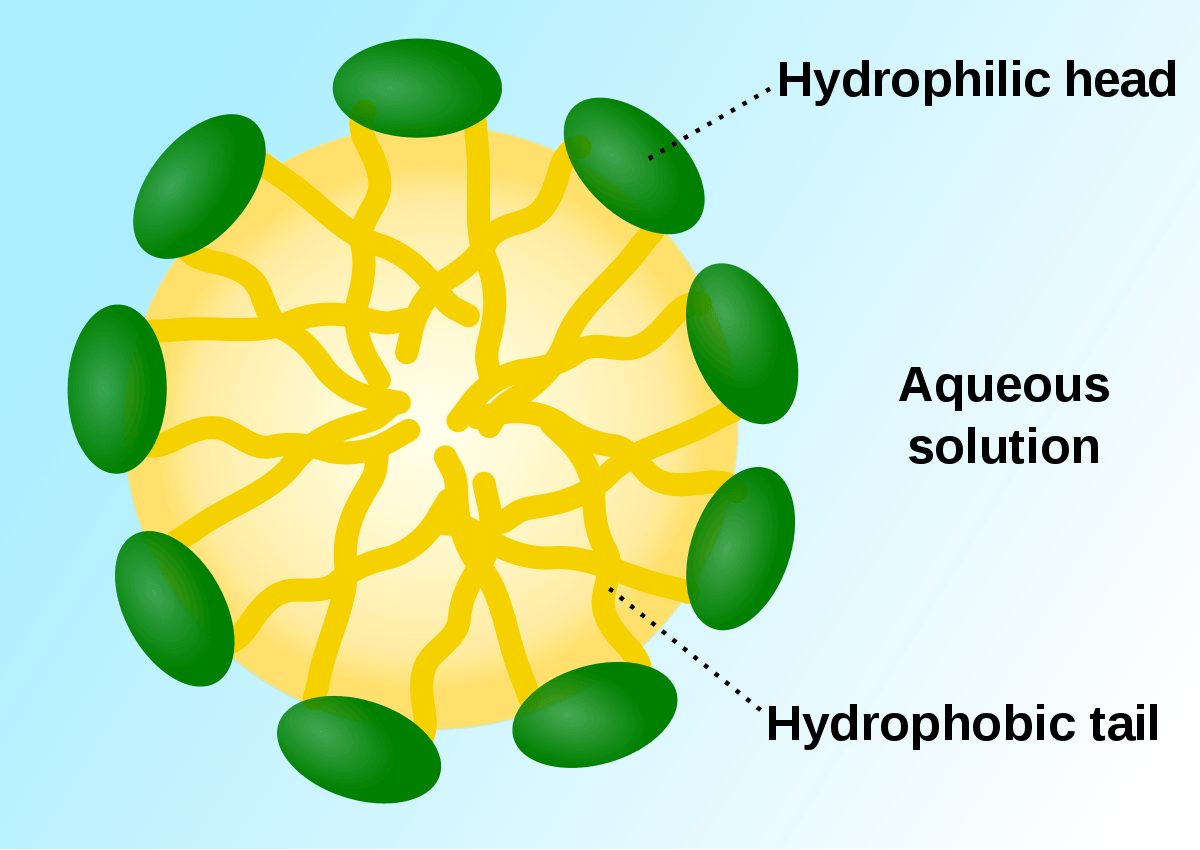
Steroids
- steroids 是另一個重要的 lipids,它的特徵就是 4 個 fused rings
- 雖然和其他 lipids 的架構幾乎不同,但他依然是 hydrophobic 以及 insoluble in water
- 有些 steroids (例如 cholesterol, 膽固醇) 會有一些 short tail
- 很多 steroids 會有 -OH functional group 出現在特定的地方
- 這類有 -OH 的 steroids 也會被認定為 alcohols,稱作 sterols
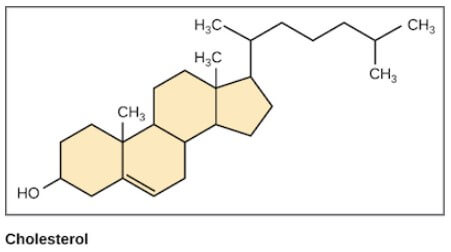
- Cholesterol 是最常見的 steroid,主要在肝產生
- 是很多 steroid hormones 的 precursor
- 例如 testosterone (睪酮), estradiol (雌二醇)
- 也是其他重要 molecules 的 precursor
- 例如 vitamin D, bile acids (膽汁酸)
- 用於從飲食中消化脂肪利用
- 或是重要的 membranes component
- 是很多 steroid hormones 的 precursor
- 血液中也會出現 cholesterol
- 可以有正面影響
- 例如在其 HDL form 可以保護人體
- 也可以有反面影響
- 在其 LDL form 可以傷害心血管健康
- 可以有正面影響
Nucleic acids
- DNA 持有從雙親繼承下來的遺傳資訊,提供一些關鍵的 instructions
- 例如要在何時、如何產生 proteins 來幫助建立 functioning cells, tissues, organisms
- DNA 是如何將這些資訊帶入 cells, organisms 的 ?
- 其實非常複雜、甚至 mind-blowing
- 會在之後的 molecular biology 章節講到
- 這邊先從 macromolecule 的角度簡單介紹 nucleic acids
Roles of DNA and RNA in cells
- Nucleic acids 主要是由多個 nucleotides 所組成的,主要有兩種類型
- deoxyribonucleic acid (DNA)
- DNA 是所有 living organism (單細胞細菌到多細胞生物) 的遺傳物質
- ribonucleic acid (RNA)
- RNA 則是某些病毒 (but technically not alive) 的遺傳物質
- deoxyribonucleic acid (DNA)
DNA in cells
- 為什麼 DNA 的名字中有 nucleic ?
- 因為 DNA 會在細胞核中被發現
- 例如 eukaryotes (真核生物,動物或植物) 的 DNA 可以在 nucleus 找到
- nucleus 通常在 membrane-bound cell 之中
- 或是在一些 organelles 中 (mitochondria, chloroplasts of plants)
- 或是 prokaryotes (原核生物,細菌) 的 DNA 可以在 nucleoid 找到
- nucleoid 則是沒有任何 membrane 保護
- 例如 eukaryotes (真核生物,動物或植物) 的 DNA 可以在 nucleus 找到
- 因為 DNA 會在細胞核中被發現
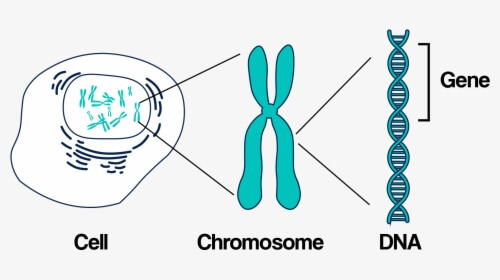
- eukaryotes 的 DNA 通常拆分成又長又直的單位,稱作 chromosomes (染色體)
- prokaryotes 的 DNA 通常就拆成比較小,而且又是 ring-shaped 的 chromosomes
- chromosome 當中包含了成千上萬的 genes
- 每個 genes 都提供了如何生產 cell 必要產物的 instruction
From DNA to RNA to proteins
- Genes 要怎麼用來生成 protein products ?
- 也就是如何指定特定的 amino acids 序列來組合特定的 protein ?
- 首先要先產生 RNA copy (transcript)
- 又稱作 messenger RNA (mRNA)
- 因為該 mRNA 會是 DNA 到 ribosomes 中間的 messenger
- 接著 molecular machines 就會讀取 mRNA 的序列來建立 proteins
- 這個 DNA 到 RNA 到 protein 的過程可以稱為 "central dogma"
- 首先要先產生 RNA copy (transcript)
- 值得一提的是,不是所有 genes 都是用來 encode proteins
- 例如 ribosomal RNAs (rRNAs) 用來作為 ribosomes 架構的元件
- 或是 transfer RNAs (tRNAs) 負責運送 amino acids 到 ribosome 來執行 protein 合成
- 還有 microRNAs (miRNAs) 作為 genes 的 regulators
- 另外還是有非常多 non-protein-coding 的 RNA
Nucleotides
- DNA 和 RNA 都是非常長的 polymers
- 由非常多的 monomers (nucleotides) 組成,所以又稱 polynucleotide
- 其中的 nucleotide 由三個部分組成
- nitrogenous base
- nitrogen-containing ring structure
- five-carbon sugar
- 這個 sugar 會在 nucleotide 的中央
- 一個 carbon 會和 phosphate group 連結
- 一個 carbon 會和 nitrogenous base 連結
- phosphate group
- nitrogenous base
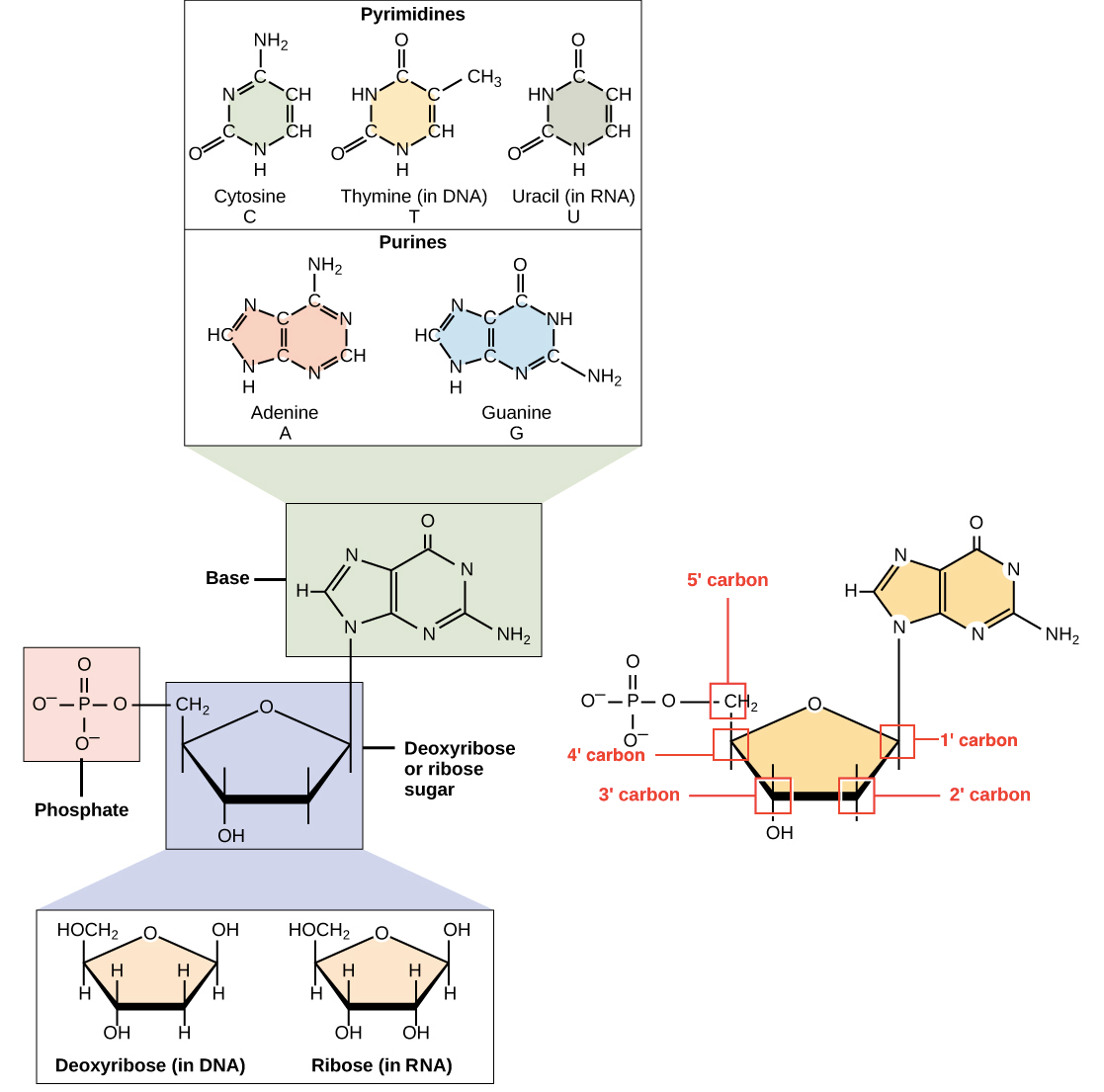
Nitrogenous bases
- nitrogenous bases 由 carbon-based 組成的 molecules
- 其中包含 nitrogen,且為 ring structures
- DNA 中的每個 nucleotide 都可能出現 4 種不同的 nitrogenous bases
- 這 4 種又可以分為 2 類
- Purine : 有 2 個 fused carbon-nitrogen rings
- Adenine (A)
- Guanine (G)
- Pyrimidine : 只有 1 個 carbon-nitrogen ring
- Thymine (T)
- Cytosine (C)
- Purine : 有 2 個 fused carbon-nitrogen rings
- 在 RNA 中,thymine 則會被另一種 pyrimidine base : uracil (U) 取代
- 所以 DNA 有 A, T, G, C
- 而在 RNA 有 A, U, G, C
- 為什麼會有 uracil (U),又或者為什麼要有 thymine ? 原因"可能"是
- 因為 uracil 比較會發生 error (比較可能跟別人 bond)
- 所以 uracil 跟 thymine 比起來 less stable
- 所以用 RNA 在進行初期的動作,可能比較適合非常多的變化
- 而在穩定後,需要較少的 error,所以就用 thymine 來取代
Sugars
- DNA 和 RNA 的 five-carbon sugar 只有一個地方有些微的不同
- 在 DNA 的 five-carbon sugar 稱為 deoxyribose
- 在 RNA 的 five-carbon sugar 稱為 ribose
- 不同的地方在五個 carbon 中的第二個 carbon
- RNA 的 2' carbon 連結著一個 hydroxyl (OH) group
- DNA 的 2' carbon 則只跟一個 hydrogen (H) 連結,所以少了氧 (deoxy)
- 不管是 DNA 還是 RNA 的 sugar 都會用 1', 2', 3', 4', 5' 來標註 carbon
- 可以看到上面的圖片
- 1' carbon 連接到 nitrogenous base
- 5' carbon 連接到 phosphate group
Phosphate
- 一個 nucleotide 可以有 1 至 3 個 phosphate groups 連結到 sugar 的 5' carbon
- 在 cell 中,一個 nucleotide 被加入到 polynucleotide chain 時本來會持有 3 個 phosphate groups
- 但在連接到 DNA 或 RNA chain 時,會損失 2 個 phosphate groups
- 所以在 DNA 或 RNA 中,每個 nucleotide 只會有 1 個 phosphate group
Polynucleotide chains

- Polynucleotide chain (DNA, RNA) 有一個重要特性就是 directionality (方向性)
- 雖然 DNA 的兩端 backbone 看起來是平行的,但其實跟馬路一樣是雙向的 (antiparallel)
- 例如左邊的 backbone 由上而下是由以下架構所連成
- "... - phosphate - sugar 5' carbon - sugar 3' carbon - phosphate - ..."
- 右邊的 backbone 就會是相反架構
- "... - phosphate - sugar 3' carbon - sugar 5' carbon - phosphate - ..."
- 而 sugar 和 phosphate 鄰居相連的線就是 phosphodiester linkage
- sugar 的 3' carbon 的 hydroxyl group 會和 phosphate 的 hydroxyl group 相連
- 這也是 dehydration synthesis 所以會釋放出水分子
Properties of DNA
- DNA 通常是以 double helix 的樣貌出現
- 也就是 2 個 complementary chains (backbone) 互相 stuck 在一起
- 這兩條 backbone 主要由 sugars 和 phosphates 組成
- 所以又可以稱為 sugar-phosphate backbone
- 中間的每一個像階梯的就是一個個的 nitrogenous base pairs
- 每個 base pair 中的兩個 bases 則是用 hydrogen bond 相連
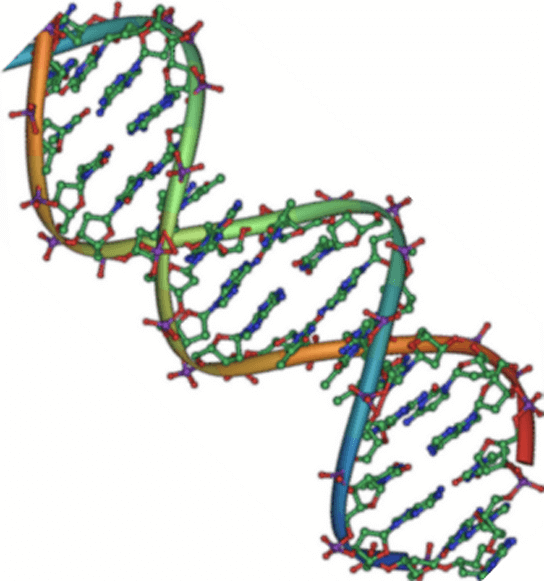
- 兩個 stands 又是以相反方向互相對應,這個現象稱為 antiparallel
- 對 DNA 的複製非常重要
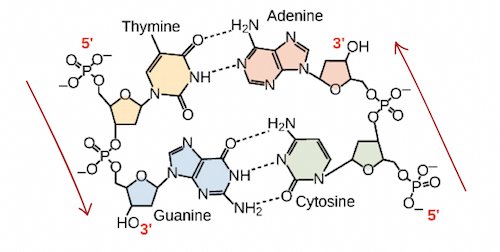
- base pair 中也不是隨便 2 個 bases 就可以組合,需考慮到 size, functional groups
- Adenine 會對應 Thymine
- Guanine 會對應 Cytosine
- 所以只要知道 DNA 的一邊,就可以簡單的猜出另外一邊
- 例如當 DNA 的一邊是
5'-AATTGGCC-3' - 那麼另外一邊一定是
3'-TTAACCGG-5'
- 例如當 DNA 的一邊是
- DNA 的 antiparallel 方式的 match 現象,稱為 complementary
Properties of RNA
- RNA 和 DNA 的結構不同,是只有一條的
- 裡面的每個 nucleotide 包含
- five-carbon ribose
- 4 nitrogenous bases (A, U, G, C)
- phosphate group
- 主要的 RNA 類別有
- messenger RNA (mRNA)
- ribosomal RNA (rRNA)
- transfer RNA (tRNA)
- regulatory RNAs
Messenger RNA (mRNA)
- mRNA 是 protein-coding gene 和 protein 產物的中間人
- 當需要製作 protein 時,RNA-polymerizing enzyme 就會來製作 RNA copy (transcript)
- 這個 RNA copy 是從 gene's DNA sequence 複製而來
- 並且 RNA 會將 DNA 資訊的 Thymine 用 Uracil 取代
- 例如 DNA sequence
5'-AATTGCGC-3'會變成 RNA sequence5'-AAUUGCGC-3'
- 例如 DNA sequence
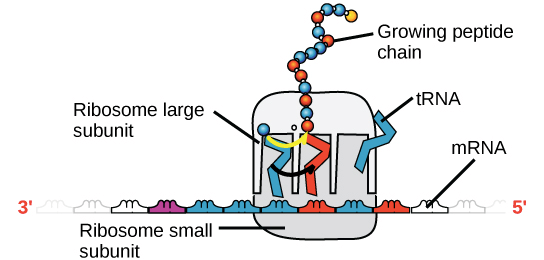
- 所以 mRNA 產生後,就會去找 ribosome (負責將一堆 amino acids 組合成 proteins)
- ribosome 讀取 mRNA 從 DNA 複製的遺傳資訊,然後就可以開始製作 proteins
- mRNA 的 nucleotides 會被三個一組的閱讀,每一組稱為一個 codon
- 每一個 codon 產出特定的 amino acid
Ribosomal RNA (rRNA)
- rRNA 是 ribosome 的主要元件
- 幫助 mRNA 找到正確的位置,讓資訊能夠正確被讀取
- 有些 rRNA 的作用也像 enzymes,幫助催化 chemical reactions
- 在這個例子中就是加速 amino acids 組成 proteins 的過程
- 幫助催化的 rRNA 可以稱作 ribozymes
Transfer RNA (tRNA)
- tRNA 也在 protein synthesis 裡面作為 carriers 的角色
- tRNA 將 amino acids 帶到 ribosome
- 確保要加入到 protein chain 的 amino acid 是符合 mRNA 的要求
- tRNA 是一個單串 RNA,但當中有許多互補的區段,這些區段互相鏈結產生雙螺旋的區間
Regulatory RNA (miRNAs, siRNAs)
- 其他沒有幫助製造 proteins 的 RNA 則來幫助調節 genes 的 expression
- 所以稱作 regulatory RNAs
- 例如有的 regulatory RNAs 會和 mRNA 結合
- 降低 mRNA 的 stability 或干擾 translation
- 幫助 cell 來降低或者是 fine-tune 這些 mRNA 的 level
- 目前還有很多 noncoding RNA 在探索中
Summary of DNA and RNA
| DNA | RNA | |
|---|---|---|
| Function | 存放 genetic information | 幫助合成 proteins 和調節 gene |
| Sugar | Deoxyribose | Ribose |
| Structure | Double helix | Usually single-stranded |
| Bases | A, T, C, G | A, U, C, G |
Proteins
- Proteins 不是單純的一種物質,而是非常多樣的存在生物體或細胞中
- 他們有不同的 size, shape, function, jobs
- 例如 structural parts, signal, messengers, metabolic enzymes, ...
- Proteins 比其他的 macromolecules 還要有更多的架構、功用
- 一個簡單的細胞可以有上千個 proteins,每個有不同的 function
- 但他們還是來自一連串的 amino acids 來組成
Types and functions of proteins
| Role | Examples | Functions |
|---|---|---|
| digestive enzyme | amylase, lipase | 分解食物養分,讓人體快速吸收 |
| transport | hemoglobin | 在血液或淋巴中運送物質 |
| structure | actin, tubulin | 幫助組織各種架構,例如 cytoskeleton |
| hormone signaling | insulin, glucagon | 調和身體系統運作 |
| defense | antibodies | 保護身體不受外界病原體攻擊 |
| contraction | myosin | 負責肌肉收縮功能 |
| storage | legume storage protein | 供給養分給成長中的胚胎 |
Amino acids
- amino acids 是產生 protein 的 monomers
- 由一個或多個 chains of amino acids 所組成的 protein 又可稱作 polypeptide
- 人體有 20 種常見的 amino acids 可以在 protein 中找到
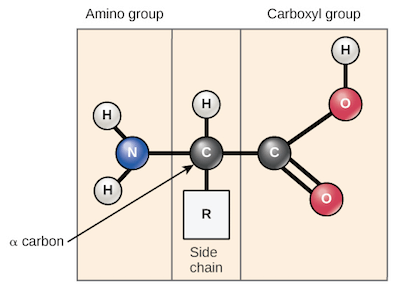
- 所有的 amino acids 都有一些共通的架構
- 左邊是 amino 的 amino group
- 右邊是 acid 的部分,是個 carboxyl group
- 中間一定會有一個 carbon 叫做 alpha carbon
- alpha carbon 會連接一個 hydrogen atom 還有 side chain
- side chain 的不同造就出不同作用的 amino acids
- 例如 R 的部分只是一個 hydrogen atom,那麼就會是 glycine
- R 的部分是 methyl group ,那麼就會是 alanine
- 上面的 amino group 和 carboxyl group 看起來呈中性,但實際中的 amino acid 不會是這種狀態
- 在 pH 7.2 - 7.4 的情況下 :
- amino group 會是 protonated (帶些微正電)
- carboxyl group 則會 deprotonated (帶些微負電)
Peptide bonds
- Protein 是一或多個 polypeptide chains 所組成
- polypeptide chain 又是由 amino acids 相連而成
- amino acids 之間是用一種 covalent bond 稱作 peptide bond 所連結在一起
- 每個 bond 是經由 dehydration synthesis 才產生的,如下圖所示
- 最尾端的 amino acid 的 carboxyl group 的 OH
- 和新來的 amino acid 的 amino group 的 H
- 兩者進行 dehydration (condensation) 合成,釋放出水分子並連結起來
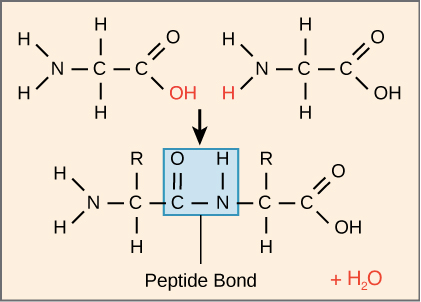
- 另外 polypeptide chain 是有 directionality 的
- 也就是 chain 有完全不同的兩端
- 有一端稱作 amino terminus (N-terminus) 有一個多的 amino group
- 另一端稱作 carboxyl terminus (C-terminus) 有一個多的 carboxyl group
- 其中 N 端在左邊,而 C 端在右邊。上圖就是一個非常短的 polypeptide 例子
Orders of Protein Structure
- Protein 中的 polypeptide, amino acids 的架構只要改變,就會連帶改變非常多功能或特性
- 這邊以煎蛋的蛋白為何會從透明變成白色不透明來舉例
- 蛋白中包含大量的 proteins (albumins)
- 這些 albumins 因為 amino acids 的架構形成 3D 的形狀
- 加熱使得 amino acid 之間的 bonds 被切開
- 一些 hydrophobic 的 amino acids 就被暴露出來
- 這些 amino acids 為了避免碰到水,所以又互相連結了起來
- 形成了 protein network 使得蛋白從透明變白
所以 protein 的形狀及架構非常重要,會關係到他的 function,
而要了解 protein 的架構,需要從 primary, secondary, tertiary, quaternary 這四個架構來了解
Primary Structure
- 這是最簡單的一層,就是以 amino acids 的排列來決定架構
- 例如以下是一個 hormone insulin,他有兩個不同的 polypeptide chain
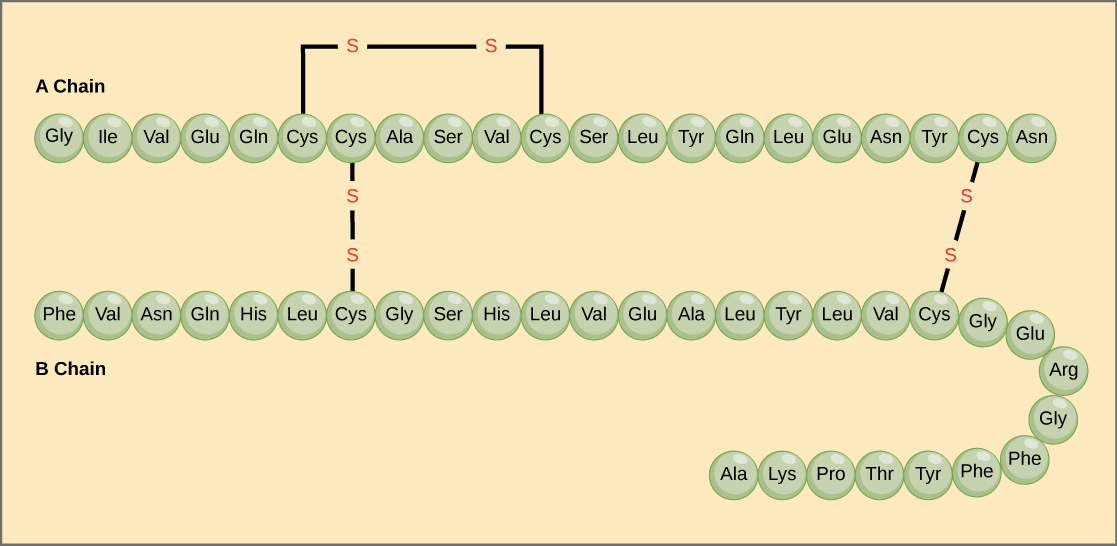
- protein 的 sequence 是 gene's DNA sequence 所提供的
- 只要 gene's DNA sequence 稍微改變,protein 中的 amino acid 就會跟著改變
- 而只要有任一個 amino acid 被改變,那整個 protein 的架構跟功能就會完全不同
- 例如 sickle cell anemia 症狀
- 在血液中運送氧氣的 hemoglobin 某個 amino acid 遭到改變
- 在 beta chain 上的第 6 個 glutamic acid 被 valine 取代掉
- 在血液中運送氧氣的 hemoglobin 某個 amino acid 遭到改變
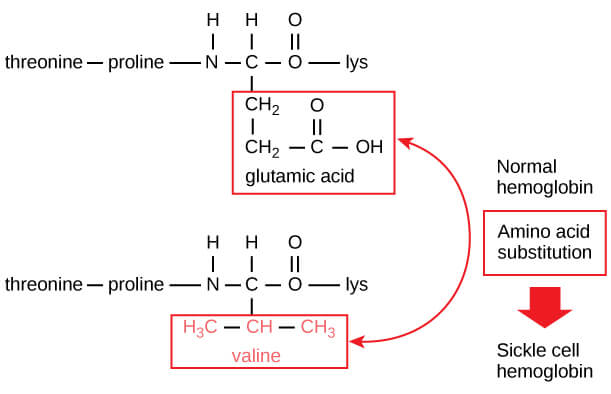
- 這還只是 hemoglobin 中 600 個 amino acids 的其中 2 個被改變而已 - 但這個改變使得 hemoglobin 的形狀完全改變 (disc to cresent) - 讓 hemoglobin 非常困難於經過血管,造成嚴重的健康問題
Secondary Structure
- 第二層則是以 protein 的 backbone 上的 atoms 互動來決定架構
- 在這一層還不包含 amino acid 中的 R groups
- 最常見的 secondary structure 為下面兩者
- 兩者都是由一邊的 carbonyl O 和一邊的 amino H 以 hydrogen bond 連結而產生
- α helix
- 例如 amino acid 1 的 carbonyl 和 amino acid 5 的 N-H 以 hydrogen bond 連結
- 這讓 polypeptide chain 產生 helical structure (curled ribbon)
- 每一圈大約有 3.6 個 amino acids
- β pleated sheet
- polypeptide chain 上的 2 個或多個 segments 透過 hydrogen bond 連結
- 形成類似 sheet 的架構,這個 sheet 可以是 parallel 也可以是 antiparallel
- α helix
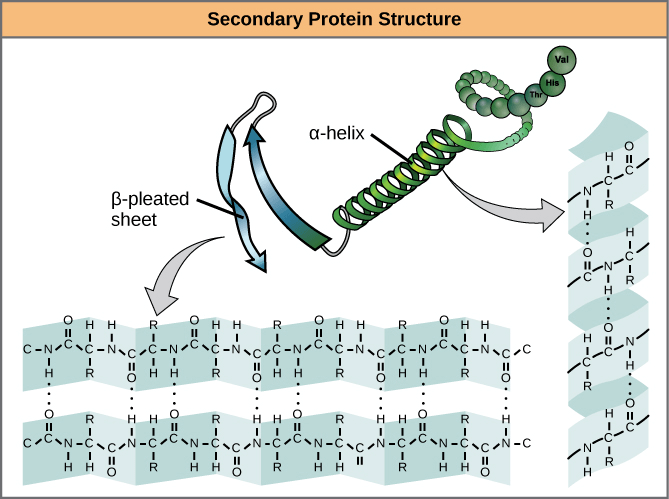
- 大部分的 amino acids 都會以上面兩種型態出現
- 但有的 amino acids 也可一次出現兩種型態,或是根本不是上面兩種型態
- 例如 amino acid proline 因為 R group 會和 amino group 連結形成 ring
- 所以他會破壞 helix 的形狀,變得 bend, unstructured
- 其他 amino acids 如 tryptophan, tyrosine, phenylalanine 有較大的 ring structure R group
- 他們常被發現於 β pleated sheet,可能因為空間較大放得下他們的 side chains
- 例如 amino acid proline 因為 R group 會和 amino group 連結形成 ring
Tertiary Structure
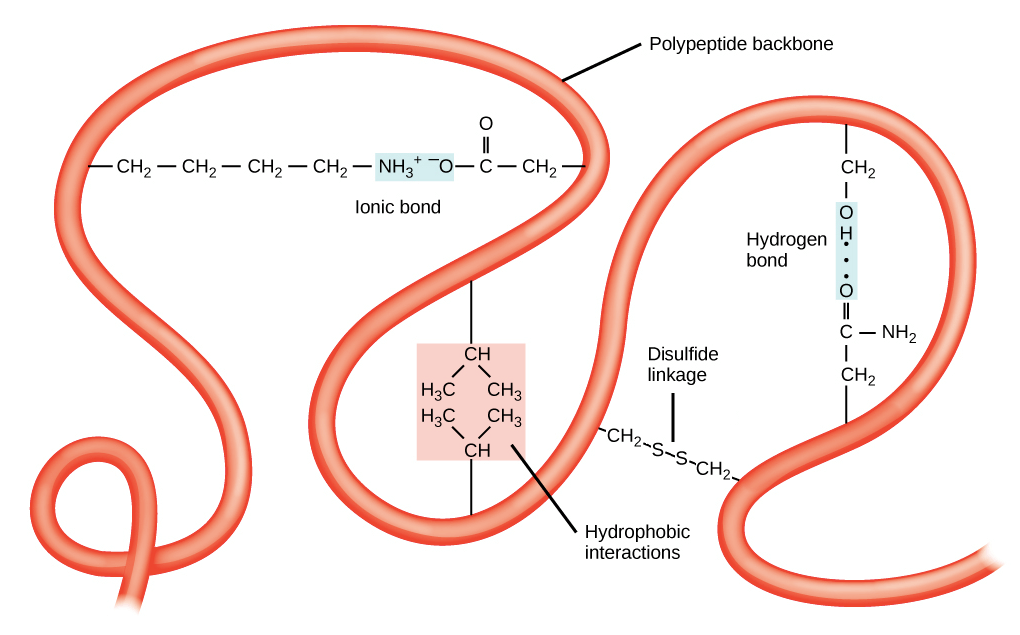
- 第三層是由 R groups 之間的反應來決定架構
- 通常是由 R group 中間 non-covalent bonds 來造成第三層改變
- hydrogen bond, ionic bond, dipole-dipole, london dispersion forces
- 例如兩邊 R group 的電極非常不同,容易形成 ionic bond
- 例如 polar R groups 容易產生 hydrogen bonds, dipole-dipole 反應
- 另一個改變第三層的重要原因是 hydrophobic interactions
- Nonpolar, hydrophobic 的 R groups 群聚起來躲在 protein 內部避免碰到水
- 讓 hydrophilic amino acids 在外部與水分子作用
- 最後一個改變第三層的是一個 covalent bond 叫做 disulfide bond
- 包含 sulfur 的 amino acid cysteines 互相透過 covalent bond 連結
- 非常堅固,可以視為 molecular "safety pins"
- 通常是由 R group 中間 non-covalent bonds 來造成第三層改變
Quaternary Structure
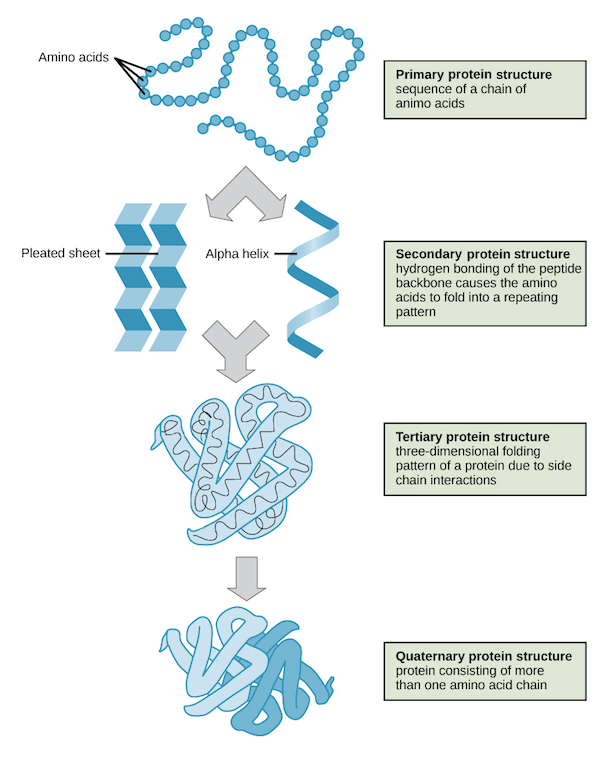
- 前三層都跟 amino acids 有關,第四層則是與 polypeptides 的排列有關
- 當 protein 只有單個 polypeptide chain 時只會有前三層架構
- 當 protein 有多個 polypeptide chains 就會出現第四層架構
- 有第四層架構的例子有
- hemoglobin (2 alpha + 2 beta)
- 運送血液中氧氣
- 還有 DNA polymerase (10 subunits)
- 一種產生新 DNA 的 enzyme
- hemoglobin (2 alpha + 2 beta)
以下圖片總結了這四層改變 protein 架構的方法
Denaturation and protein folding
- Protein 組起來的 3D 架構會因為溫度或是 pH 而改變
- Protein 會因此被分解,變回簡單的 amino acid string
- Protein 失去架構的這個過程稱為 denaturation
- Denatured proteins 是毫無功用的 (non-functional)
- 有些 denaturation 是 reversible,有的是 permanent
- 因為 primary structure 未受到改變,回到原本的環境或許能讓 protein 恢復形狀
- 但有的 denaturation 是永遠的,例如蛋白煮熟就回不去了